Что такое ффл в медицине
Что такое ффл в медицине
О недостаточности того или иного органа мы обычно говорим, когда он не в состоянии в полном объеме выполнять свои функции. Функция сердца заключается в выбросе в аорту количества крови, адекватного потребностям организма. Таким образом, сердечная недостаточность (СН) может быть определена как нарушение структуры и функции сердечной мышцы, ведущее к неспособности переносить кислород в том количестве, которое необходимо для тканевого метаболизма [12].
Основной причиной является повреждение миокарда, ведущее к патологическому ремоделированию желудочка вследствие расширения камеры и нарушения сократимости. Эти изменения приводят к снижению сердечного выброса, уменьшению перфузии органов и активации компенсаторных нейрогормональных систем [39].
Главными проявлениями сердечной недостаточности являются одышка и утомляемость. Эти симптомы могут ухудшить функциональные возможности и качество жизни пациентов [8].
Если объем поражения достаточно велик, то в первый момент произойдет падение выброса крови из левого желудочка и снижение ее давления на стенки аорты и крупных сосудов. Это приведет к активации расположенных там барорецепторов. Ответом будет немедленная активация симпато-адреналовой системы (САС). Стимуляция находящихся в сердце β-рецепторов ведет к увеличению ЧСС и повышению сократимости миокарда. Стимуляция находящихся в стенке сосудов рецепторов катехоламинами вызывает реакцию централизации кровотока, а за счет спазма вен увеличивается возврат крови к сердцу во время диастолы [39].
Активация САС ведет к активации ренин-ангиотензин-альдостероновой системы (РААС) [3, 12].
Ренин является ферментом превращающим физиологически неактивный ангиотензиноген в ангиотензин-1. Последний под влиянием ангиотензинпревращающего фермента превращается в одно из наиболее биологически активных веществ – ангиотензин-2. Его образование существенно усиливает спазм сосудов, обусловленный реакцией централизации кровотока. Помимо вазоконстрикции ангиотензин-2 вызывает рост клеток, способствует апоптозу и,что важно в данном случае, увеличивает синтез альдостерона. Альдостерон способствует реабсорбции жидкости в дистальных отделах нефрона. Таким образом, возникающая в ответ на повреждение миокарда активация САС и РААС приводит к постепенному накоплению избытка жидкости в организме. Этот процесс требует времени и достигает клинически значимого эффекта только спустя несколько суток после острой сердечной катастрофы [12].
Несмотря на серьезные достижения в лечении хронической сердечной недостаточности, терапия острой сердечной недостаточности остается практически неизменной. В частности, лечение острой сердечной недостаточности во многом основывается не на доказательной медицине, а на эмпирических данных [15].
Острая сердечная недостаточность (ОСН) – синдром, характеризующийся застойными явлениями по малому и/или большому кругу кровообращения вследствие увеличения давления наполнения левого желудочка с или без уменьшения сердечного выброса. Риск смерти и повторной госпитализации больных ОСН после выписки из стационара остаётся высоким и составляет от 10 до 20%, и от 20 до 30% – в течение180 дней, соответственно [15].
Если отбросить все остальное, то все, что требует организм от сердца, это поддержать кровоток на должном уровне. Сердечный выброс (СВ) – это производное частоты сердечных сокращений (ЧСС) и ударного объема (УО) сердца (объема крови, выталкиваемого из желудочков в ходе каждого сокращения). Увеличение ЧСС является важным ранним компенсаторным механизмом, нормальным ответом сердца на снижение СВ. У здоровых молодых людей СВ возрастает при росте ЧСС до 170–180 уд./мин, а затем начинает снижаться (так как продолжительность диастолы становится слишком короткой для того, чтобы обеспечить достаточное наполнение желудочков). У пожилых пациентов с дисфункцией сердца падение СВ наблюдается при ЧСС менее 150 уд./мин. Имеется три основных фактора, определяющих УО желудочков: преднагрузка, постнагрузка и сократимость миокарда [10, 34].
Преднагрузка характеризует напряжение стенки желудочка в конце диастолы (при максимальном наполнении сердца перед сокращением). Это напряжение трудно измерить, а в качестве «суррогата» (или максимально приближенного показателя) обычно используется конечно-диастолическое давление (КДД). Эта величина определяется венозным возвратом и дает представление о давлении заполнения желудочков [7].
Сократимость — работа, производимая сердцем на данном уровне преднагрузки и постнагрузки. Определяется максимальной скоростью, с которой желудочек может генерировать изменение давления за единицу времени. Понятие «инотропизм» используется для объяснения усиления работы, выполняемой сердцем, независимо от ЧСС, преднагрузки и постнагрузки [7].
Постнагрузка — это напряжение, которое должно быть сгенерировано в стенке желудочка для того, чтобы выбросить кровь во время систолы в артериальную систему. Этот показатель находится под сильным влиянием сопротивления артерий — системного сосудистого сопротивления [7].
В интактном сердце длина мышечных волокон пропорциональна конечному диастолическому объему (КДО) желудочков. Поэтому увеличение наполнения желудочков во время диастолы (или рост преднагрузки) вызывает рост силы последующего сокращения и увеличение УО и СВ. Вот почему факторы, способствующие увеличению объема внутрисосудистой жидкости (а именно – задержка натрия и воды) являются одними из основных компенсаторных механизмов СН. В этом случае увеличение объема внутрисосудистой жидкости приводит к росту венозного возврата к обоим желудочкам, увеличению их КДО и, в конце концов, к повышению УО. Исходя из того, что увеличение преднагрузки способствует росту УО и СВ, можно было бы предположить, что лечение, направленное на повышение объема внутрисосудистой жидкости, было бы полезным в тех случаях, когда функция желудочков угнетена. Но основная проблема такого «лечения» заключается в том, какой именно объем внутрисосудистой жидкости необходим для оптимальной преднагрузки и как его определить у конкретного пациента [10].
В начальной стадии СН снижение сократимости желудочка компенсируется повышением преднагрузки (КДО и КДД), что приводит к нарастанию ударного объема; кроме того, увеличивается частота сердечных сокращений (ЧСС). По мере прогрессирования СН повышение КДД в желудочке все меньше сказывается на ударном объеме; вместе с тем растет давление в венах малого и большого круга кровообращения, вызывая симптомы застоя. Повышается напряжение в стенке желудочка и снижается коронарный кровоток в диастолу, вследствие ухудшается энергетический баланс миокарда [2].
Сопряжение возбуждения и сокращения в миокарде
Когда мембранный потенциал достигает уровня –65 мВ, открываются потенциалзависимые кальциевые каналы L-типа, обеспечивающие формирование входящего кальциевого тока, который ускоряет деполяризацию кардиомиоцитов. В результате активируются потенциалзависимые кальциевые ионные каналы мембраны T-трубочек и рианодиновые рецепторы саркоплазматического ретикулума. Резкое повышение концентрации ионов кальция в саркоплазме устраняет тропомиозиновую блокаду взаимодействия актина и миозина и запускает процесс сокращения кардиомиоцитов. Следовательно, сократимость сердечной мышцы непосредственно зависит от силы входящего кальциевого тока [3, 5]. Существует и другой механизм поступления больших количеств ионов кальция в цитоплазму рабочего кардиомиоцита при его возбуждении. Он обеспечивается сопряженным транспортом ионов кальция и натрия через мембрану, то есть натрий-кальциевым обменом. Во время диастолы натрий-кальциевая помпа активно удаляет из клетки ионы кальция в обмен на ионы натрия. При возбуждении кардиомиоцита направление натрий-кальциевого обмена меняется на противоположное: ионы кальция активно переносятся в клетку, тогда как ионы натрия, напротив, удаляются, и в результате концентрация ионов кальция в цитоплазме кардиомиоцита возрастает [5, 26].
Комплекс актина и тропонина
Несмотря на то, что ионы кальция, соединяясь с ТрС (тропонин С), дают сигнал к запуску цикла поперечных мостиков, есть доказательства, что начинается не только сигнальный процесс включения-выключения. Чтобы понять роль кальция, нужно описать молекулярную структуру комплекса актина и тропонина. Тонкие филаменты состоят из двух актиновых частей, сплетенных в спираль; обе части находятся на более тяжелой молекуле тропомиозина, которая играет роль стержня. С равными интервалами к этим закручивающимся структурам прикреплены три регуляторных белка, называемых тропониновым комплексом. ТрС состоит из короткого N-концевого домена и четырех кальций?связывающих EF-рук, объединенных попарно в глобулярный N-концевой и С-концевой домены [6, 20].
Распространение потенциала действия по мышечному волокну в начале систолы приводит к выходу ионов кальция из саркоплазматического ретикулума и повышению концентрации свободного кальция в цитоплазме. Присоединение кальция ко второй EF-руке ТрС приводит к изменению конформации всего N-концевого домена белка. При этом появление на поверхности N-концевого домена ТрС гидрофобной области, с которой связывается регуляторный домен ТрI (тропонин I). Он перемещается на новое место на тонком филаменте, ослабляя таким образом взаимодействие между ТрТ (тропонин Т) и тропомиозином. В результате тропомиозин перемещается по тонкому филаменту, и устраняется торможение, оказываемое тропомиозином на взаимодействие актина и миозина [6, 20].
АТФ как источник энергии для сокращения
Сокращение сердечной мышцы происходит благодаря скольжению тонких актиновых филаментов относительно толстых миозиновых. Данный процесс обеспечивается за счет циклического АТФ-зависимого взаимодействия миозина и актина. Миозин связывает и гидролизует АТФ до АДФ и неорганического фосфата, но при этом практически не способен избавляться от накопившихся в активном центре продуктов АТФазной реакции. Головка миозина, содержащая в своем составе АДФ и фосфат, способна слабо взаимодействовать с актином, что активирует процесс освобождения фосфата из активного центра миозина. Освобождение неорганического фосфата (а вслед за этим и АДФ) из активного центра миозина сопровождается изменением ориентации «шейки» головки миозина, протягиванием нити актина относительно головки миозина и развитием натяжения. Связывание новой молекулы АТФ приводит к диссоциации миозина от актина и после гидролиза АТФ происходит очередное циклическое присоединение головки миозина к актину и осуществляется новый «шаг» миозина по актину [3].
В цикле поперечных мостиков АТФ выполняет две разные роли:
1) гидролиз АТФ поставляет энергию для движения поперечного мостика;
2) связывание (но не гидролиз) АТФ с миозином сопровождается отделением миозина от актина и создает возможность повторения цикла поперечных мостиков [1].
Миозиновая АТФазная активность реагирует на воздействие кальция следующим образом: во время цикла сокращения сердца концентрация кальция повышается, что ведет к повышению миозиновой АТФазной активности в несколько раз, а также к повышению присоединения кальция к ТрС [3].
Подходы к лечению сердечной недостаточности
Подходы к лечению сердечной недостаточности менялись неоднократно. В 50-60 годах 20 века основной терапией считали инотропную стимуляцию сердца, в 70-х упор делался на борьбу с задержкой жидкости, в 80-е надежды связывали с уменьшением нагрузки на сердце за счет использования вазодилататоров, в 80-х годах синтезировала ингибитор фосфодиэстеразы III (ФДЭ III), за двойной эффект – инотропное и вазодилатирующее, названное инодилататорами. Начиная с 90-х основой лечения стало подавление избыточной активации нейрогуморальных систем [12].
Механизм действия инотропных препаратов
Препараты, обычно используемые для достижения положительного иноторопного эффекта, включают катехоламины, напр. добутамин, и ингибиторы ФДЭ III, напр. милринон. У этих веществ разные точки приложения, но они, в конечном счете, запускают каскад событий, приводящих к улучшению сократимости путем увеличения концентрации внутриклеточного кальция. Взаимодействие катехоламинов с β1-адренорецепторами на поверхности кардиомиоцитов активирует аденилатциклазу, катализирующую превращение АТФ в цАМФ. цАМФ активирует протеинкиназу А, которая, в свою очередь, фосфорилирует внутриклеточные субстраты, включая потенциалзависимые кальциевые каналы L-типа, фосфоламбан, ТрI. Фосфорилирование потенциалзависимых кальциевые каналов L-типа стимулирует поступление кальция в цитозоль. Это является триггером для открытия рианодиновых рецепторов саркоплазматического ретикулума и мышечного сокращения (положительное инотропное действие катехоламинов и ингибиторов ФДЭ III). В то же время фосфорилирование фосфоламбана активирует SERCA2, что приводит к обратному захвату кальция саркоплазматическим ретикулумом во время диастолы. Это обусловливает люзитропный эффект катехоламинов и ингибиторов ФДЭ III. Также фосфорилирование ТрI уменьшает сродство миофиламентов к кальцию и способствует релаксации. Сердечные гликозиды, напр. дигоксин, селективно и обратимо ингибируют сарколеммальную натрий-калиевую АТФазу кардиомиоцитов, повышая т.о. концентрацию натрия внутри клетки, что, в свою очередь, ингибирует выкачивание кальция из клетки натрий-кальциевой помпой. Омекатив мекарбил – новый препарат – активатор миозина. Активирует миозиновую АТФазу [26, 32, 33].
За исключением дигоксина, не оказывающего эффекта на общую смертность, имеющиеся препараты с положительным инотропным действием, включая агонисты β1-адренорецепторов, ингибиторы ФДЭ III, оказались вредны для долгосрочного лечения СН, т.к. они могут способствовать развитию злокачественных желудочковых тахиаритмий и увеличить риск внезапной сердечной смерти. Также короткосрочное применение ингибиторов ФДЭ III ассоциируется с частым возникновением таких осложнений, как фибрилляция предсердий, гипотензия, особенно если у пациента имеется ишемия миокарда ввиду ишемической кардиомиопатии. Причины столь разочаровывающих открытий кроются в том, что, несмотря на различные точки приложения, все эти препараты усиливают сократимость миокарда путем увеличения внутриклеточного уровня цАМФ в кардиомиоцитах или благодаря его усиленному синтезу (при приеме агонистов β1-адренорецепторов), или снижению скорости его деградации (при приеме ингибиторов ФДЭ III), что усиливает высвобождение кальция из саркоплазматического ретикулума в цитозоль. Увеличение внутриклеточного кальция, в свою очередь, ведет к временному улучшению сократимости миокарда ценой увеличения потребления миокардом энергии и потребности в кислороде, что в итоге ведет к клеточной смерти. Более того, увеличение концентрации цАМФ и изменение обмена кальция кардиотоксичны и могут привести к нарушениям ритма [17].
Инотропные препараты существенно увеличивают энергетические затраты кардиомиоцитов. Увеличение внутриклеточного кальция ведет к временному улучшению сократимости миокарда ценой увеличения потребления миокардом энергии и потребности в кислороде, что в итоге ведет к клеточной смерти. Более того, увеличение концентрации цАМФ и изменение обмена кальция кардиотоксичны и могут привести к нарушениям ритма [19].
Было проведено значительное количество исследований, направленных на поиск нового инотропного препарата, действие которого не имеет под собой увеличения кальция в клетке. В теории такой препарат должен был усиливать сократимость без увеличения потребности миокарда в кислороде и без риска возникновения аритмий. Т.к. связь между уровнем внутриклеточного кальция и взаимодействием миофиламентов может быть нарушена ввиду таких патофизиологических состояний, как ишемия, ацидоз, сепсис или гипотермия, разрабатываемый препарат должен был укреплять эту связь, но не изменять внутриклеточную концентрацию кальция. Все «сенситизаторы кальция», включая левосимендан, пимобендан, EMD 57033, ORG 30029, MCI-154 и другие, имеют способность усиливать сократимость миокарда путем увеличения чувствительности миофиламентов к кальцию с различной интенсивностью, с помощью различных механизмов и точек приложения и различной степенью одновременного ингибирования фосфодиэстеразы III. Среди этих препаратов левосимендан наиболее эффективен в лечении хронической и острой левожелудочковой недостаточности [20].
Регистрационное свидетельство препарату левосимендан впервые было предоставлено в 2000 году в Швеции. В настоящее время левосимендан обладает
регистрационным свидетельством в более чем 50 странах по всему миру, при
этом установлено, что на декабрь 2014 года более 800 000 пациентов получили
инфузию препарата в рамках рутинной клинической практики [14].
Левосимендан – сенситизатор кальция, инодилататор, разработанный для внутривенного применения у пациентов, госпитализированных с острой декомпенсированной сердечной недостаточностью (ОДСН). Фармакологические действия левосимендана включают:
а) повышение сократимости сердца благодаря сенситизации тропонина С к кальцию;
б) вазодилатацию вследствие открытия калиевых каналов саркоплазматической мембраны в гладкомышечных клетках сосудов;
в) кардиопротекцию благодаря открытию митохондриальных калиевых каналов в кардиомиоцитах [25, 26, 31].
Функции внешнего дыхания: показания, противопоказания, методика исследования
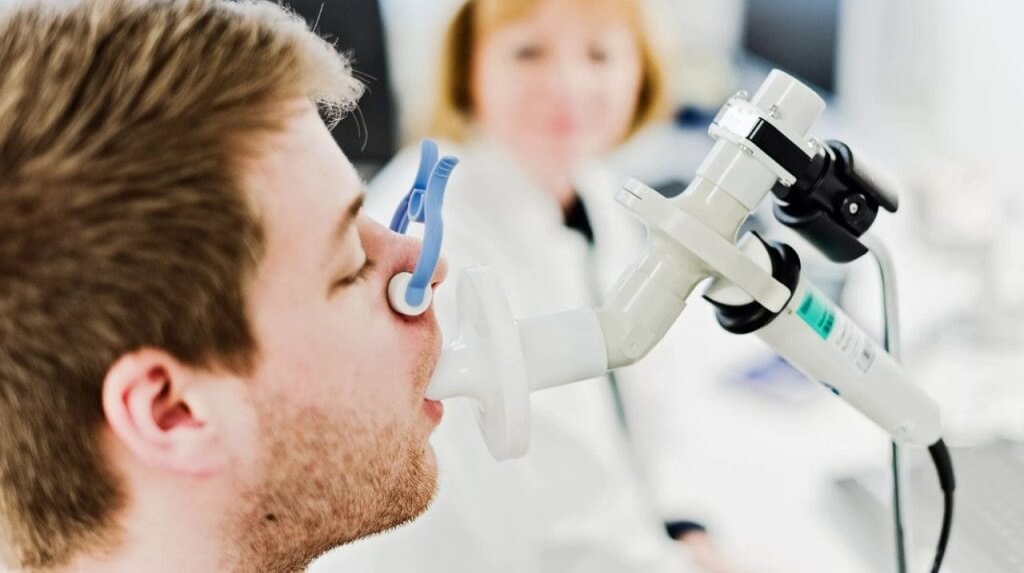
Внешнее дыхание – термин, обозначающий циркуляцию воздуха, направленную по системе дыхательных путей. Отклонения от нормы в процессе указывают на заболевания. Оценка функции внешнего дыхания способна выявить нарушения в работе легких, а так же бронхов, диагностирует скрытые патологии.
ФВД: что это такое?
Исследование ФВД – процедура, определяющая вентиляционную способность легких. Тест дает представление о полном и остаточном объеме воздуха в легких, скорости движения воздуха во внутренних органах. Врачи сравнивают результаты диагностики с показателями нормы функции внешнего дыхания и делают вывод о прогрессировании заболевания, эффективности лечения, ставят диагноз.
Оценка ФВД безопасна и проводится взрослым и детям. Тест помогает выявить причину одышки, контролировать состояние организма у спортсменов, людей, относящихся к группе риска (курящие, работники вредных производств). Исследование необходимо и пациентам, готовящихся к операции на легких и бронхах.
Показания и противопоказания
Обязательным тест считается при наличии показаний:
Плановое обследование проходят курильщики и спортсмены перед стартом соревнований.
Как медицинское исследование, анализ ФВД имеет противопоказания. Тест не проводится при наличии у пациента туберкулеза, пневмоторакса, умственных и психических расстройств, кровотечений в дыхательных органах, глаукомы. Исследованию не подлежат люди, перенесшие аневризму аорты, инфаркт или инсульт, дети до 5 лет и пожилые в возрасте после 75 лет.
Что показывает функция внешнего дыхания
На монитор аппарата во время теста выводится ряд показателей, которые подлежат расшифровке специалистом. Поскольку уровень подготовки и физической активности индивидуальны для каждого пациента, оценка результатов также будет разниться.
Разъясняя пациенту особенности функционирования его дыхательной системы, доктор может прокомментировать, что показывает функция внешнего дыхания. К основным показателям относятся:
Основываясь на перечисленных показателях теста, врач диагностирует патологии плевры, легких и бронхов, мышц, отвечающих за дыхание.
ФВД: подготовка к исследованию
Чтобы пройти обследование, вы можете обратиться в наш центр и получить консультацию опытного кардиолога. Врач расскажет, как проводится функция внешнего дыхания, и как правильно подготовиться к анализу.
Перед диагностической процедурой необходимо исключить факторы, влияющие на результат. За несколько дней до теста запрещено:
Пациенту заранее заготавливает легкую одежду, не сдавливающую живот и грудь.
Метод исследования функции внешнего дыхания в МЦОЗ:
Процесс, как делают и как проверяют функцию внешнего дыхания, зависит от выбранного способа. Каждый из них отличается технически и по количеству определяемых показателей.
Для распознавания хронической обструктивной болезни легких и бронхиальной астмы может применяться спирометрическая проба с бронхлитиками. Тест выполняется для оценки значимости препятствия.
Детям до 5 лет исследование ФВД не проводят: крик, плач, негативные эмоции искажают данные. Школьники проходят тест в кабинете функциональной диагностики, он оснащен игрушками, тут царит благожелательная атмосфера. Найти подход к ребенку может педиатр. Детям до 9 лет понять инструкции врача помогают картинки. Тесты проводят 2-3 раза. Если результаты мало отличаются, исследование считают информативным.
ФВД: расшифровка, показатели
Цель исследования – выявление аномалий ФВД. Для этого врач анализирует полученные показатели и ставит диагноз. Есть различные типы нарушений функции внешнего дыхания:
Результаты исследований выводятся на монитор в виде цифровых данных и графиков. Самостоятельно пациенту расшифровать их сложно: для этого требуются медицинские знания. Лучше обратиться к врачу, который грамотно прокомментирует данные теста.
Сделать это можно в Международном центре охраны здоровья. У нас работают квалифицированные доктора, которые проведут обследование легких, расшифруют показатели и назначат курс лечения.
Если пациент обращается в клинику впервые, врач осмотрит его, расспросит о жалобах и назначит один из типов исследования ФВД. Перед процедурой он расскажет о ходе процедуры, предоставит инструкции, чтобы пациент чувствовал себя комфортно.
Традиционно обследованием легочной ткани пациента занимается пульмонолог, лечением детей и подростков – детский пульмонолог. Когда причина ухудшения состояния не определена, поможет терапевт. Он поставит предварительный диагноз, направит к пульмонологу или кардиологу. Обращаясь в нашу клинику, пациенты могут быть уверены, что им окажут высококвалифицированную помощь.
Для записи на исследование звоните нам или заполняйте на интернет-ресурсе специальную форму. Операторы выберут комфортное для клиента время, сориентируют по стоимости, напомнят о подготовке к тесту.
Гипервентиляционный синдром и дисфункциональное дыхание
Клинические особенности, диагностические критерии гипервентиляционного синдрома (ГВС) и дисфункционального дыхания (ДД) недостаточно знакомы широкому кругу врачей [1, 2, 3]. К одной из исторических вех, связанной с понятиями о функциональных нарушениях
Клинические особенности, диагностические критерии гипервентиляционного синдрома (ГВС) и дисфункционального дыхания (ДД) недостаточно знакомы широкому кругу врачей [1, 2, 3]. К одной из исторических вех, связанной с понятиями о функциональных нарушениях дыхания, относят 1871 год, когда Да Коста (Da Costa Jacob, 1833–1900), американский врач, принимавший участие в Гражданской войне США, применил термин «гипервентиляционый синдром» (ГВС) у пациентов с так называемым «солдатским сердцем». С тех пор для характеристики дыхательных расстройств предлагались различные альтернативные определения: «дыхательный невроз», «нейрореспираторная дистония», «респираторный синдром», «респираторная дискинезия», «идиопатическая гипервентиляция», «нейрореспираторный синдром», «неустойчивое дыхание» и др. Однако указанные термины не получили широкого признания. Они являются достаточно общими и не отражают особенностей нарушений дыхания у конкретного больного [4]. Перечисленные определения нередко связывают с понятием «непонятная одышка» (unexplained dyspnea).
ГВС встречается в 6–11% от числа пациентов общей практики. Соотношение мужчин и женщин составляет 1:4, 1:5; чаще наблюдается в 30–40 лет, но возможно развитие в других возрастных группах, включая детей и пожилых. L. Lum (1987) подчеркивал, что «каждый врач в течение недели может встретить хотя бы одного больного с ГВС». Врачи различных специальностей — невропатологи, кардиологи, пульмонологи, психиатры — могут наблюдать у своих пациентов явления гипервентиляции. Острое течение ГВС встречается значительно реже, чем хроническое, и составляет лишь 1–2% от общего числа больных [2, 6, 7].
Причины развития ГВС довольно многочисленны. Это неврологические и психические расстройства, вегетативные нарушения, болезни органов дыхания, некоторые заболевания сердечно-сосудистой системы, органов пищеварения, экзогенные и эндогенные интоксикации, лекарственные средства (салицилаты, метилксантины, β-агонисты, прогестерон) и др. Считается, что в 5% случаев ГВС имеет только органическую природу, в 60% случаев — только психогенную, в остальных — комбинации этих причин [6].
Важной особенностью развития ГВС является то обстоятельство, что если причины, являющиеся триггерными, устраняются, то гипервентиляция, которая уже не соответствует требованиям конкретной ситуации, сохраняется, сохраняется и гипокапния. Происходит стабилизация гипокапнических нарушений газообмена и формируется «порочный круг» ГВС, который начинает циркулировать автономно, и симптомы могут персистировать достаточно долго — феномен «махового колеса». Эти изменения реакции дыхания указывают на уязвимую систему контроля дыхания, которая не способна поддержать нормальное парциальное давление углекислого газа в крови (РСО2) и кислотно-щелочной гомеостаз [8, 9, 10, 11].
В основе развития клинических проявлений ГВС лежат гипокапнические нарушения газообмена [2, 3, 10]. Среди множества клинических проявлений ГВС одышка является ведущей жалобой и встречается практически в 100% случаев. Одышка может быть единственным клиническим проявлением, но чаще сочетается с другими симптомами.
Основные клинические проявления ГВС
Респираторные: одышка, вздохи, зевота, сухой кашель.
Общие: снижение трудоспособности, слабость, утомляемость, субфебрилитет.
Кардиальные: кардиалгия, экстрасистолия, тахикардия.
Психоэмоциональные: тревога, беспокойство, бессонница.
Гастроэнтерологические: дисфагия, боли в эпигастрии, сухость во рту, аэрофагия, запоры.
Неврологические: головокружение, обмороки, парестезии, тетания (редко).
Мышечные: мышечная боль, тремор.
Диагностика ГВС в первую очередь опирается на знание врачей самых различных специальностей об особенностях клинической картины ГВС. ГВС должен устанавливаться только после проведения дифференциальной диагностики с другими заболеваниями, протекающими с синдромом одышки. Полиморфизм клинических проявлений ГВС вызывает диагностические проблемы. Назначаются многочисленные обследования, дорогостоящие, ненужные, а иногда и опасные для больного. L. Lum (1987), обсуждая диагностические проблемы, называет среди врачебных ошибок бесполезные абдоминальные операции, операции на позвоночнике и других органах, инвазивные исследования, проводимые не без риска, и, что еще хуже, такие диагнозы, как эпилепсия и инфаркт миокарда. Взаимосвязи гипокапнии и ассоциированных с ней симптомов являются чрезвычайно сложными. Многие врачи при регистрации у больных низких значений РСО2 автоматически устанавливают диагноз ГВС, что является неправильным. Известно, что явления гипокапнии могут быть у больных рестриктивными легочными процессами, при лихорадочных состояниях, сердечной патологии, однако при этом «классических» гипокапнических жалоб может и не быть. И наоборот, так называемые гипокапнические жалобы, например тревога, одышка, парестезии и др., встречаются у пациентов с нормокапнией.
В практической медицине больной с ГВС — это пациент, предъявляющий жалобы на одышку, которая не соответствует данным объективного осмотра, показателям клинико-инструментальных исследований дыхания, с диспропорциональной, непонятной одышкой, субъективное восприятие которой является довольно тягостным. К сожалению, при отсутствии достоверных объяснений одышки больные обычно направляются для консультаций в различные лечебные учреждения. В конечном итоге они и формируют основной контингент альтернативной медицины, различных псевдоспециалистов «по тренировке правильного дыхания».
Исследование функции внешнего дыхания, имеющее важное значение в дифференциальной диагностике одышки, не помогает в верификации функциональных нарушений дыхания. Основным подтверждением ГВС служит выявление гипокапнических нарушений газообмена. Снижение РСО2 — прямое свидетельство альвеолярной гипервентиляции. Однако исходная гипокапния у больных с ГВС встречается не так часто. Поэтому в тех случаях, когда у пациента с предположительным ГВС в условиях покоя определяются нормальные значения углекислоты, рекомендуется определение изменений уровня СО2 при различных провокационных тестах. К «золотому стандарту» диагностики ГВС относят пробу с произвольной гипервентиляцией.
Департаментом пульмонологии университета г. Наймиген (Голландия) разработан Наймигенский опросник (Nijmegen questionnaire) для выявления физиологических показателей дизрегуляции вентиляции, сопоставимых с ГВС (табл.). Анкета содержит 16 пунктов, которые оцениваются по 5-балльной шкале (0 — никогда, 4 — очень часто). Минимальные и максимальные достижимые числа — 0 и 64 соответственно.
Данный опросник нашел свое применение прежде всего для скрининг-диагностики ГВС. Существует положение, согласно которому использование данного опросника позволяет корректно предсказывать ГВС в 90% от всех случаев [2, 12].
В последние годы в клиническую практику начинает внедряться понятие «дисфункциональное дыхание» (ДД). Приоритет внедрения термина принадлежит Ван Диксхорну (J. van Dixhoorn), который привел его в работе Hyperventilation and dysfunctional breathing (1997). Основанием для этого явилось понимание, что при функциональных нарушениях дыхания возможны различные изменения паттерна дыхания и значений РCO2, а не только гипокапнические расстройства, характерные для ГВС. ДД может проявляться также быстрым, аритмичным, поверхностным дыханием, частыми вздохами, преобладанием грудного типа дыхания.
Одной из сложных и дискуссионных проблем в пульмонологии является понимание взаимоотношений ГВС, ДД и бронхиальной астмы (БА) [15–18]. С. И. Овчаренко и др. (2002) у 22 из 80 больных БА выявили нарушения дыхания, соответствующие критериям ГВС. Сведений относительно встречаемости дисфункциональных нарушений дыхания при астме немного. Установлено, что среди лиц с диагнозом БА и по крайней мере с одним предписанием антиастматического препарата 29% имеют клинические признаки ДД [19]. Указывается, что ДД может усиливать симптомы БА и приводить к избыточному назначению лекарств.
Достаточно сложным является понимание механизмов развития дисфункциональных расстройств дыхания при БА; существует ряд предположений. К достаточно обоснованным факторам развития гипервентиляции относят тревожные расстройства. Использование больными бронходилататоров (β-2-агонисты, теофиллин), которые обладают эффектами стимуляции дыхания, также относят к факторам развития гипервентиляции. Обсуждается роль изменений перцепции одышки при БА. Анализ существующих проблем взаимосвязи ДД и БА провел M. Morgan (2002), представив следующие ключевые положения:
В зависимости от установления особенностей ДД должна осуществляться и программа лечения больных. При выявлении ГВС релаксирующие методы дыхательной гимнастики проводятся под руководством опытных инструкторов, назначаются β-адреноблокаторы, бензодиазепины [5, 22, 23]. При явлениях гиповентиляции — массаж дыхательных мышц, использование дыхательных тренажеров. Выявление ГВС при БА указывает на необходимость применения методов коррекции функциональных нарушений дыхания. Релаксирующие дыхательные упражнения за счет неспецифических механизмов дыхательного тренинга улучшают качество жизни у этих больных.
По вопросам литературы обращайтесь в редакцию.
В. Н. Абросимов, доктор медицинских наук, профессор
Рязанский ГМУ им. акад. И. П. Павлова, Рязань