в каком виде в земной коре встречаются соединения железа назовите 3 4 минерала
Железо. Свойства железа и его соединений.
Железо
Положение в периодической системе химических элементов
Элемент железо расположен в побочной подгруппе VIII группы (или в 8 группе в современной форме ПСХЭ) и в четвертом периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение атома железа
Электронная конфигурация железа в основном состоянии :
+26Fe 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6
Железо проявляет ярко выраженные магнитные свойства.
Физические свойства
Железо – металл серебристо-белого цвета, с высокой химической активностью и высокой ковкостью. Обладает высокой тепло- и электропроводностью.

Температура плавления 1538 о С, температура кипения 2861 о С.
Нахождение в природе
Железо довольно распространено в земной коре (порядка 4% массы земной коры). По распространенности на Земле железо занимает 4-ое место среди всех элементов и 2-ое место среди металлов. Содержание в земной коре — около 8%.
В природе железо в основном встречается в виде соединений:

Магнитный железняк Fe3O4 или FeO·Fe2O3 (магнетит).
(изображение с портала emchi-med.ru)
В природе также широко распространены сульфиды железа, например, пирит FeS2.

Встречаются и другие минералы, содержащие железо.
Способы получения
Железо в промышленности получают из железной руды, гематита Fe2O3 или магнетита (Fe3O4или FeO·Fe2O3).
В печь загружают руду, кокс и флюсы.
Шихта – смесь исходных материалов, а в некоторых случаях и топлива в определённой пропорции, которую обрабатывают в печи.
Каменноугольный кокс – это твёрдый пористый продукт серого цвета, получаемый путем коксования каменного угля при температурах 950—1100 °С без доступа воздуха. Содержит 96—98 % углерода.
Флюсы – это неорганические вещества, которые добавляют к руде при выплавке металлов, чтобы снизить температуру плавления и легче отделить металл от пустой породы.
Шлак – расплав (а после затвердевания – стекловидная масса), покрывающий поверхность жидкого металла. Шлак состоит из всплывших продуктов пустой породы с флюсами и предохраняет металл от вредного воздействия газовой среды печи, удаляет примеси.
В печи кокс окисляется до оксида углерода (II):
2C + O2 → 2CO
Затем нагретый угарный газ восстанавливает оксид железа (III):
Процесс получения железа – многоэтапный и зависит от температуры.
Наверху, где температура обычно находится в диапазоне между 200 °C и 700 °C, протекает следующая реакция:
Ниже в печи, при температурах приблизительно 850 °C, протекает восстановление смешанного оксида железа (II, III) до оксида железа (II):
Встречные потоки газов разогревают шихту, и происходит разложение известняка:
Оксид железа (II) опускается в область с более высоких температур (до 1200 o C), где протекает следующая реакция:
FeO + CO → Fe + CO2
Углекислый газ поднимается вверх и реагирует с коксом, образуя угарный газ:
CO2 + C → 2CO

2. Также железо получают прямым восстановлением из оксида водородом:
При этом получается более чистое железо, т.к. получаемое железо не загрязнено серой и фосфором, которые являются примесями в каменном угле.
3. Еще один способ получения железа в промышленности – электролиз растворов солей железа.
Качественные реакции
Качественные реакции на ионы железа +2.
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Видеоопыт взаимодействия раствора сульфата железа (II) с раствором гидроксида натрия (качественная реакция на ионы железа (II)) можно посмотреть здесь.
Гидроксид железа (II) на воздухе буреет, так как окисляется до гидроксида железа (III):
– ионы железа +2 окрашивают раствор в светлый желто-зеленый цвет.
– взаимодействие с красной кровяной солью K3[Fe(CN)6] – также качественная реакция на ионы железа +2. При этом образуется синий осадок «турнбулева синь».
Видеоопыт взаимодействия раствора хлорида железа (II) с раствором гексацианоферрата (III) калия (качественная реакция на ионы железа (II)) можно посмотреть здесь.
Качественные реакции на ионы железа +3

3NaOH + FeCl3 → Fe(OH)3 + 3NaCl
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором гидроксида натрия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
– ионы железа +3 окрашивают раствор в светлый желто-оранжевый цвет.
– взаимодействие с желтой кровяной солью K4[Fe(CN)6] ионы железа +3. При этом образуется синий осадок «берлинская лазурь».
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором гексацианоферрата (II) калия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
В последнее время получены данные, которые свидетельствуют, что молекулы берлинской лазури идентичны по строению молекулам турнбулевой сини. Состав молекул обоих этих веществ можно выразить формулой Fe4[Fe2(CN)6]3.
– при взаимодействии солей железа (III) с роданидами раствор окрашивается в кроваво-красный цвет.
FeCl3 + 3NaCNS → Fe(CNS)3 + 3NaCl
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором роданида калия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
Химические свойства
1.1. Железо реагирует с галогенами с образованием галогенидов. При этом активные неметаллы (фтор, хлор и бром) окисляют железо до степени окисления +3:
2Fe + 3Cl2 → 2FeCl3
Менее активный йод окисляет железо до степени окисления +2:
1.2. Железо реагирует с серой с образованием сульфида железа (II):
Fe + S → FeS
Fe + P → FeP
1.4. С азотом железо реагирует в специфических условиях с образованием нитрида дижелеза:
1.5. Железо реагирует с углеродом и кремнием с образованием карбида и силицида:
3Fe + C → Fe3C
1.6. При взаимодействии с кислородом железо образует окалину – двойной оксид железа (II, III):
При пропускании кислорода через расплавленное железо возможно образование оксида железа (II):
2Fe + O2 → 2FeO
2. Железо взаимодействует со сложными веществами.
2.1. При обычных условиях железо с водой практически не реагирует. Раскаленное железо может вступать в реакцию при температуре 700-900 о С с водяным паром:
3 Fe 0 + 4 H2 + O → Fe +3 3O4 + 4 H2 0
В воде в присутствии кислорода или во влажном воздухе железо медленно окисляется (корродирует):
2.2. Железо взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой). При этом образуются соль железа со степенью окисления +2 и водород.
Fe + 2HCl → FeCl2 + H2↑
2.3. При обычных условиях железо не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат железа (III) и вода:
2.4. Железо не реагирует при обычных условиях с концентрированной азотной кислотой также из-за пассивации. При нагревании реакция идет с образованием нитрата железа (III), оксида азота (IV) и воды:
С разбавленной азотной кислотой железо реагирует с образованием оксида азота (II):
При взаимодействии железа с очень разбавленной азотной кислотой образуется нитрат аммония:
Fe + CuSO4 → FeSO4 + Cu
Еще пример : простое вещество железо восстанавливает железо до степени окисления +2 при взаимодействии с соединениями железа +3:
2FeCl3 + Fe → 3FeCl2
Оксид железа (II)
Оксид железа (II) – это твердое, нерастворимое в воде вещество черного цвета.
Способы получения
Оксид железа (II) можно получить различными методами :
1. Частичным в осстановлением оксида железа (III).
Или частичным восстановлением оксида железа (III) угарным газом:
Еще один пример : восстановление оксида железа (III) железом:
2. Разложение гидроксида железа (II) при нагревании :
Химические свойства
1. При взаимодействии оксида железа (II) с кислотными оксидами образуются соли.
FeO + SO3 → FeSO4
FeO + 2HCl → FeCl2 + H2O
3. Оксид железа (II) не взаимодействует с водой.
4. Оксид железа (II) малоустойчив, и легко окисляется до соединений железа (III).
При взаимодействии с разбавленной азотной кислотой образуется оксид азота (II). Реакция идет при нагревании:
FeO + CO → Fe + CO2
Оксид железа (III)
Оксид железа (III) – это твердое, нерастворимое в воде вещество красно-коричневого цвета.
Способы получения
Оксид железа (III) можно получить различными методами :
1. Окисление оксида железа (II) кислородом.
2. Разложение гидроксида железа (III) при нагревании :
Химические свойства
1. При взаимодействии оксида железа (III) с кислотными оксидами и кислотами образуются соли.
3. Оксид железа (III) не взаимодействует с водой.
4. Оксид железа (III) окисляется сильными окислителями до соединений железа (VI).
Нитраты и нитриты в щелочной среде также окисляют оксид железа (III):
Также оксид железа (III) восстанавливается водородом:
Железом можно восстановить оксид железа только до оксида железа (II):
Оксид железа (III) реагирует также с некоторыми другими сильными восстановителями.
Fe2O3 + 3NaH → 3NaOH + 2Fe
6. Оксид железа (III) – твердый, нелетучий и амфотерный. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Оксид железа (II, III)
Оксид железа (II, III) (железная окалина, магнетит) – это твердое, нерастворимое в воде вещество черного цвета.
Фото с сайта wikipedia.ru
Способы получения
Оксид железа (II, III) можно получить различными методами :
1. Горение железа на воздухе:
2. Частичное восстановление оксида железа (III) водородом или угарным газом :
3. При высокой температуре раскаленное железо реагирует с водой, образуя двойной оксид железа (II, III):
Химические свойства
Свойства оксида железа (II, III) определяются свойствами двух оксидов, из которых он состоит: основного оксида железа (II) и амфотерного оксида железа (III).
1. При взаимодействии оксида железа (II, III) с кислотными оксидами и кислотами образуются соли железа (II) и железа (III).
Еще пример : оксид железа (II, III) взаимодействует с разбавленной серной кислотой.
2. Оксид железа (II, III) взаимодействует с сильными кислотами-окислителями (серной-концентрированной и азотной).
Разбавленной азотной кислотой окалина окисляется при нагревании:
Также оксид железа (II, III) окисляется концентрированной серной кислотой:
Также окалина окисляется кислородом воздуха :
3. Оксид железа (II, III) не взаимодействует с водой.
4. Оксид железа (II, III) окисляется сильными окислителями до соединений железа (VI), как и прочие оксиды железа (см. выше).
Также железная окалина восстанавливается водородом:
Оксид железа (II, III) реагирует также с некоторыми другими сильными восстановителями (йодидами и сульфидами).
Гидроксид железа (II)
Способы получения
1. Гидроксид железа (II) можно получить действием раствора аммиака на соли железа (II).
2. Гидроксид железа (II) можно получить действием щелочи на соли железа (II).
FeCl2 + 2KOH → Fe(OH)2↓ + 2KCl
Химические свойства
Гидроксид железа (II) взаимодействует с пероксидом водорода:
При растворении Fe(OH)2 в азотной или концентрированной серной кислотах образуются соли железа (III):
4. Г идроксид железа (II) разлагается при нагревании :
Гидроксид железа (III)
Способы получения
1. Гидроксид железа (III) можно получить действием раствора аммиака на соли железа (III).
2. Окислением гидроксида железа (II) кислородом или пероксидом водорода:
3. Гидроксид железа (III) можно получить действием щелочи на раствор соли железа (III).
FeCl3 + 3KOH → Fe(OH)3↓ + 3KCl
Видеоопыт получения гидроксида железа (III) взаимодействием хлорида железа (III) и гидроксида калия можно посмотреть здесь.
Например: бромид железа (III) реагирует с карбонатом натрия. При этом выпадает осадок гидроксида железа (III), выделяется углекислый газ и образуется бромид натрия:
Взаимодействие хлорида железа (III) с сульфитом, например, калия — очень интересная реакция. Во-первых, в некоторых источниках указывается, что в ней таки может протекать необратимый гидролиз. Но для ЕГЭ лучше считать, что при этом протекает ОВР. Во-вторых, ОВР можно записать в разных видах:
Также допустима такая запись:
Химические свойства
3. Гидроксид железа (III) взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—ферриты, а в растворе реакция практически не идет. При этом гидроксид железа (III) проявляет кислотные свойства.
4. Г идроксид железа (III) разлагается при нагревании :
Видеоопыт взаимодействия гидроксида железа (III) с соляной кислотой можно посмотреть здесь.
Соли железа
Нитраты железа
Нитрат железа (II) при нагревании разлагается на оксид железа (III), оксид азота (IV) и кислород:
Нитрат железа (III) при нагревании разлагается также на оксид железа (III), оксид азота (IV) и кислород:
Гидролиз солей железа
Растворимые соли железа, образованные кислотными остатками сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. частично:
I ступень: Fe 3+ + H2O ↔ FeOH 2+ + H +
II ступень: FeOH 2+ + H2O ↔ Fe(OH )2 + + H +
Однако сульфиты и карбонаты железа (III) и их кислые соли гидролизуются необратимо, полностью, т.е. в водном растворе не существуют, а разлагаются водой:
При взаимодействии соединений железа (III) с сульфидами протекает ОВР:
2FeCl3 + 3Na2S → 2FeS + S + 6NaCl
Более подробно про гидролиз можно прочитать в соответствующей статье.
Окислительные свойства железа (III)
Соли железа (III) под проявляют довольно сильные окислительные свойств. Так, при взаимодействии соединений железа (III) с сульфидами протекает окислительно-восстановительная реакция.
Например : хлорид железа (III) взаимодействует с сульфидом натрия. При этом образуется сера, хлорид натрия и либо черный осадок сульфида железа (II) (в избытке сульфида натрия), либо хлорид железа (II) (в избытке хлорида железа (III)):
2FeCl3 + 3Na2S → 2FeS + S + 6NaCl
2FeCl3 + Na2S → 2FeCl2 + S + 2NaCl
По такому же принципу соли железа (III) реагируют с сероводородом:
2FeCl3 + H2S → 2FeCl2 + S + 2HCl
2FeCl3 + 2KI → 2FeCl2 + I2 + 2KCl
Однако, соли железа со степенью окисления +3 в этом ряду являются небольшим исключением. Ведь для железа характерны две степени окисления: +2 и +3. И железо со степенью окисления +3 является более сильным окислителем. Таким образом, условно говоря, железо со степенью окисления +3 расположено в ряду активности после меди. И соли железа (III) могут реагировать еще и с металлами, которые расположены правее железа! Но до меди, включительно. Вот такой парадокс.
И еще один момент. Соединения железа (III) с этими металлами реагировать будут, а вот соединения железа (II) с ними реагировать не будут. Таким образом, металлы, расположенные в ряду активности между железом и медью (включая медь) при взаимодействии с солями железа (III) восстанавливают железо до степени окисления +2. А вот металлы, расположенные до железа в ряду активности, могут восстановить железо и до простого вещества.
А вот реакция нитрата железа (III) с цинком протекает уже по привычному механизму. И железо восстанавливается до простого вещества:
Где встречается железо в природе
Железо — самый распространенный после алюминия металл на земном шаре; оно составляет около 5% земной коры. Встречается железо в виде различных соединений: оксидов, сульфидов, силикатов. В свободном виде железо находят в метеоритах, изредка встречается самородное железо (феррит) в земной коре как продукт застывания магмы.
Железо входит в состав многих минералов, из которых слагаются месторождения железных руд.
Основные рудные минералы железа:
Гематит (железный блеск, красный железняк) — Fe2O3 (до 70% Fe);
Магнетит (магнитный железняк) — Fe3O4 (до 72,4% Fe);
Гидрогетит — FeOOH*nH2O (лимонит) — (около 62% Fe);
Месторождения железных руд образуются в различных геологических условиях; с этим связано разнообразие состава руд и условий их залегания. Железные руды разделяются на следующие промышленные типы:
Бурые железняки — руды водной окиси железа (главный минерал — гидрогетит), 30-55% железа.
Красные железняки, или гематитовые руды (главный минерал — гематит, иногда с магнетитом), 51-66% железа.
Магнитные железняки (главный минерал — магнетит), 50-65% железа.
Сидеритовые или карбонатные осадочные руды, 30-35% железа.
Силикатные осадочные железные руды, 25-40% железа.
Большие запасы железных руд находятся на Урале, где целые горы (например Магнитная, Качканар, Высокая и др.) образованы магнитным железняком. Большие залежи железных руд имеются вблизи Курска, на Кольском полуострове, в Западной и Восточной Сибири, на дальнем Востоке. Богатые залежи имеются на Украине.
Железо является также одним из наиболее распространенных элементов в природных водах, где среднее содержание его колеблется в интервале 0,01-26 мг/л.
Железо в природе (4,7% в Земной коре)

Чаще всего железо находят в богатых металлом рудах, которые можно относительно легко добывать и перерабатывать. В чистом виде железо находили только в метеоритах, а в соединениях оно присутствует в сульфидах, силикатах и оксидах.
Характеристика железа
Физические свойства
Железо – это серебристо-белый металл с сероватым оттенком. В чистом виде пластичен, но непрочен. При добавлении в него различных добавок (например, углерода) твердость и хрупкость сплава повышается. Железо хорошо проводит электричество, тепло и обладает мощными магнитными свойствами, то есть под действием магнитного поля оно намагничивается и потом само становится магнитом.
Железо особенно важно для живых организмов. Оно способствует дыхательным процессам и входит в состав гемоглобина крови (477 мг/л). Это значит, что железо участвует в процессе доставки кислорода от органов дыхания к тканям.
Находясь в воде и на влажном воздухе железо меркнет и ржавеет, а при температуре 1539°С легко плавится и поддается ковке. При высоких температурах железо реагирует с паром воды.
Железо образует 300 разнообразных минералов (карбонаты, сульфиды и т.д.) и энергично мигрирует в земной коре. Его называют металлом земных недр, так как он копится в кристаллизации магмы.
Химические свойства
Железо — металл со средней степенью химической активности. На воздухе, на нем образуется защитная пленка, которая препятствует коррозии и ржавлению. Если воздух влажный, железо окисляется и покрывается ржавчиной.
Растворяется в разведенной соляной или серной кислотах, с выделением водорода. Вытесняет из растворов солей металлы. Во время нагревания взаимодействует с неметаллами.
Соединения и нахождение железа в природе
В естественных водах, среднее содержание железа (в интервале 0,01-26 мг/л). Кроме того, животные особи, бактерии и растения содержат его в своих организмах. Даже в тканях и внутренних органах людей есть железо, поступающее в организм вместе с едой. Потребность в нем для взрослого человека составляет 11-30мг. Избыток железа приводит к гемохроматозу и серьезным нарушениям внутренних органов.
Так как месторождения железных руд возникают в разных геологических условиях, то и состав руд и условия их расположения разнообразны.
Железо содержится во многих рудах:
• гематит (железный блеск, красный железняк),
• пирит (серный колчедан) и гетит,
• магнетит (магнитный железняк),
• сидерит и гидрогенит.
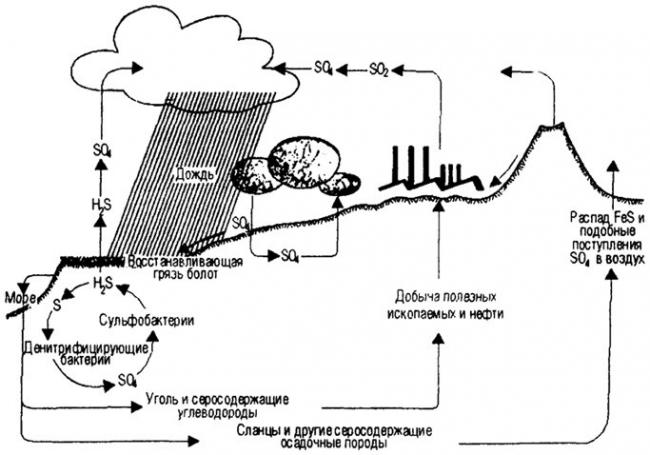
Круговорот железа в природе
(На примере круговорота серы и других соединений в природе)
За счет жизнедеятельности железобактерий (нитевидные бактерии и одиночные железобактерии) происходит круговорот железа в природе. Они окисляют железо до гидроксида железа, а углерод получают из углекислоты. Таким образом, железобактерии получают энергию для своей жизнедеятельности, а после смерти осаждаются в почве в виде болотной руды.
Области применения железа
В чистом виде железо непрочно, поэтому практически не применяется. Его используют для выработки электромагнитов, как катализатор химических реакций и др.
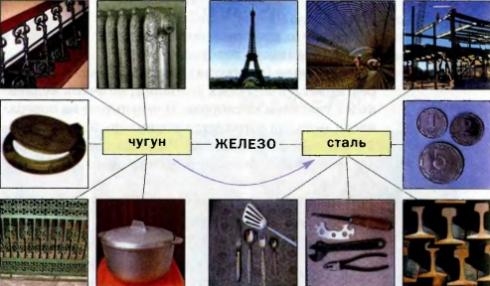
Основное применение этот металл находит в виде сплавов. На их долю приходится 95% всей металлопродукции. Железо основной компонент стали и чугуна. В стали меньше углерода, чем в чугуне, и поэтому она более пластична и устойчива к резким ударным нагрузкам железа.
Так же железо входит в состав никелевых и других сплавов, использующихся в электротехнике, железо-воздушных аккумуляторах и железо — никелевых аккумуляторах.
На основе железа производятся материалы, которые могут выдерживать действие низкой и повышенной температуры, агрессивной среды, ядерных излучений, вакуума и высоких давлений и т. п.
Железо относится к группе тех металлов, которые очень широко применяются во всех областях народного и бытового хозяйства. Чугун и сталь стали основой современной техники. С их участием произошло развитие тяжелой промышленности, разнообразного наземного транспорта и др.
Большие запасы железа в России, Австралии, Канаде, Казахстане, Индии, Франции, США, Венесуэле и ЮАР.
Где встречается железо в природе
Железо – химический элемент
1. Положение железа в периодической таблице химических элементов и строение его атома
Железо — это d- элемент VIII группы; порядковый номер – 26; атомная масса Ar ( Fe ) = 56; состав атома: 26-протонов; 30 – нейтронов; 26 – электронов.
Схема строения атома:
Электронная формула: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2
Металл средней активности, восстановитель:
Основные степени окисления: +2, +3
2. Распространённость железа
Железные руды довольно широко распространены на Земле. Названия гор на Урале говорят сами за себя: Высокая, Магнитная, Железная. Агрохимики в почвах находят соединения железа.
Железо входит в состав большинства горных пород. Для получения железа используют железные руды с содержанием железа 30-70% и более.
Основными железными рудами являются :
магнетит (магнитный железняк) – Fe3O4 содержит 72% железа, месторождения встречаются на Южном Урале, Курской магнитной аномалии:
гематит (железный блеск, кровавик)– Fe2O3 содержит до 65% железа, такие месторождения встречаются в Криворожском районе:
лимонит (бурый железняк) – Fe2O3*nH2O содержит до 60% железа, месторождения встречаются в Крыму:
пирит (серный колчедан, железный колчедан, кошачье золото) – FeS2 содержит примерно 47% железа, месторождения встречаются на Урале.
3. Роль железа в жизни человека и растений
Биохимики открыли важную роль железа в жизни растений, животных и человека. Входя в состав чрезвычайно сложно построенного органического соединения, называемого гемоглобином, железо обусловливает красную окраску этого вещества, от которого в свою очередь, зависит цвет крови человека и животных. В организме взрослого человека содержится 3 г чистого железа, 75% которого входит в состав гемоглобина. Основная роль гемоглобина – перенос кислорода из легких к тканям, а в обратном направлении – CO2.
Железо необходимо и растениям. Оно входит в состав цитоплазмы, участвует в процессе фотосинтеза. Растения, выращенные на субстрате, не содержащем железа, имеют белые листья. Маленькая добавка железа к субстрату – и они приобретают зеленый цвет. Больше того, стоит белый лист смазать раствором соли, содержащей железо, и вскоре смазанное место зеленеет.
Так от одной и той же причины – наличия железа в соках и тканях – весело зеленеют листья растений и ярко румянятся щеки человека.
4. Физические свойства железа.
Железо – это серебристо-белый металл с температурой плавления 1539 о С. Очень пластичный, поэтому легко обрабатывается, куется, прокатывается, штампуется. Железо обладает способностью намагничиваться и размагничиваться, поэтому применяется в качестве сердечников электромагнитов в различных электрических машинах и аппаратах. Ему можно придать большую прочность и твердость методами термического и механического воздействия, например, с помощью закалки и прокатки.
Восстановлением из оксидов углём или оксидом углерода (II), а также водородом:
6. Химические свойства железа
Как элемент побочной подгруппы железо может проявлять несколько степеней окисления. Мы рассмотрим только соединения, в которых железо проявляет степени окисления +2 и +3. Таким образом, можно говорить, что у железа имеется два ряда соединений, в которых оно двух- и трехвалентно.
1) На воздухе железо легко окисляется в присутствии влаги (ржавление):
2) Накалённая железная проволока горит в кислороде, образуя окалину — оксид железа (II,III) — вещество чёрного цвета:
3) При высокой температуре (700–900°C) железо реагирует с парами воды:
4) Железо реагирует с неметаллами при нагревании:
5) Железо легко растворяется в соляной и разбавленной серной кислотах при обычных условиях:
6) В концентрированных кислотах – окислителях железо растворяется только при нагревании
На холоде концентрированные азотная и серная кислоты пассивируют железо!
7) Железо вытесняет металлы, стоящие правее его в ряду напряжений из растворов их солей.
8) Качественные реакции на
Основная часть получаемого в мире железа используется для получения чугуна и стали — сплавов железа с углеродом и другими металлами. Чугуны содержат около 4% углерода. Стали содержат углерода менее 1,4%.
Чугуны необходимы для производства различных отливок — станин тяжелых машин и т.п.
Задания для закрепления
Железо в природе
Железо (Ferrum); ат. вес 55,85 — самый распространенный после алюминия металл на земном шаре, составляющий 4,2% веса земной коры. Встречается железо исключительно в виде различных соединений: окислов, сернистых соединений, силикатов. В свободном состоянии железо находят только в падающих на землю метеоритах.
Важнейшими железными рудами являются: магнитный железняк Fe3О4, красный железняк Fe2О3, бурый железняк 2Fe2О3• 3Н2О и шпатовый железняк FeCО3. Встречающийся в больших количествах железный колчедан FeS2 редко применяется в металлургии, так как железо из него получается очень низкого качества, из-за большого содержания серы. Не представляя интереса для металлургии, железный колчедан имеет тем не менее значительное применение — он служит исходным сырьем для получения серной кислоты.
В пределах СНГ месторождения железных руд находятся на Урале, где целые горы (например, Магнитная, Качканар, Высокая и др.) образованы магнитным железняком превосходного качества. Не менее богатые залежи находятся в Криворожском районе и на Керченском полуострове. Криворожские руды, которыми питается украинская металлургическая промышленность, состоят из красного железняка, керченские — из бурого железняка. Большие залежи железных руд имеются близ Курска, в области так называемой Курской магнитной аномалии. Огромные запасы железной руды обнаружены также в недрах Кольского полуострова, в Западной и Восточной Сибири и на Дальнем Востоке. Общее количество железных руд в СНГ составляет больше половины мировых запасов.
Из всех металлов, добываемых человеком, железо имеет наибольшее значение в нашей жизни. Вся современная техника связана с применением железа и его сплавов. Насколько важную роль играет железо, видно уже из того, что количество добываемого железа приблизительно в 20 раз превосходит добычу всех остальных металлов, вместе взятых.
Добыча железа особенно быстро росла в прошлом столетии. Еще в начале XIX в. мировая выплавка чугуна равнялась всего 0,8 млн. т в год, а к концу XIX в. она составляла уже 66 млн. т в год. В 1929 г. выплавка стали в капиталистических странах достигла 110,0 млн. т, после чего резко упала в годы кризиса (до 44,8 млн. т. в 1932 г.), затем снова повысилась и в 1937 г. составляла 112,8 млн. т. В 1957 г. в капиталистических странах было выплавлено 155 млн. т чугуна и 218 млн. т стали.
Вы читаете, статья на тему Железо в природе
Двойкам нет
Железо. Распространенность железа в природе. Биологическая роль железа
Второй важный химический элемент после кислорода, свойства которого будут изучаться, — это Ферум. Железо является металлическим элементом, который образует простое вещество — железо. Железо входит в состав восьмой группы побочной подгруппы периодической системы. Согласно номеру группы максимальная валентность железа должна составлять восемь, однако в соединениях Ферум чаще проявляет валентность два и три, а также известные соединения с валентностью железа шесть. Относительная атомная масса железа равно пятьдесят шесть.
По распространенной в составе земной коры Ферум занимает среди металлических элементов второе место после алюминия. Массовая доля железа в земной коре составляет почти пять процентов. В самородном состоянии железо встречается очень редко, обычно лишь в виде метеоритов. Именно в этом виде наши предки и смогли впервые познакомиться с железом и оценить его как очень хороший материал для изготовления орудий труда. Считается, что железо является главной составляющей ядра земного шара. Чаще Ферум встречается в природе в составе руд. Важнейшими из них являются: магнитный железняк (магнетит) Fe3O4, красный железняк (гематит) Fe2O3, бурый железняк (лимонит) Fe2O3 · nH2O, железный колчедан (пирит) FeS2, шпатовый железняк (сидерит) FeСO3, гетит FeO (OH). В водах многих минеральных источников содержится Fe (НСO3) 2 и некоторые другие соли железа.
Железо является жизненно важным элементом. В организме человека, как и животных, феррум присутствует во всех тканях, однако наибольшая его часть (примерно три грамма) сосредоточена в кровяных шариках. Атомы железа занимают центральное положение в молекулах гемоглобина, им гемоглобин обязан своей окраской и способностью присоединять отщеплять кислород. Железо участвует в процессе переноса кислорода от легких к тканям организма. Суточная потребность организма в Ферум составляет 15-20 мг. Общая его количество попадает в организм человека с растительной пищей и мясом. При потере крови потребность в Ферум превышает количество, которое человек получает с пищей. Недостаток железа в организме может привести к состоянию, которое характеризуется уменьшением количества эритроцитов и гемоглобина крови. Медицинские препараты железа следует принимать только по назначению врача.