что такое в химии k2o
Оксид калия
| Оксид калия | |
 | |
| Общие | |
|---|---|
| Химическая формула | K2O |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 94.20 г/моль |
| Плотность | 2.35 г/см³ |
| Термические свойства | |
| Температура плавления | 740 °C |
| Классификация | |
| Рег. номер CAS | 12136-45-7 |
СодержаниеФизические свойстваОксид калия K2O — бледно-жёлтое, иногда бесцветное, редко встречающееся вещество. Содержится в некоторых видах удобрений и цемента. Химические свойстваПроизводствоОксид калия производят взаимодействием кислорода и калия, в результате реакции образуется пероксид калия, K2O2. Обогащением пероксида калием получают оксид: [2] Более удобным способом является нагревание нитрата калия с металлическим калием: Гидроксид калия не может быть обезвожен до оксида. См. такжеСсылкиПолезноеСмотреть что такое «Оксид калия» в других словарях:оксид калия — (K2O) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN potassium oxide … Справочник технического переводчика Оксид натрия — Оксид натрия бинарное неорганическое вещество, имеющее формулу и относящееся к классу основных оксидов. Оксид натрия … Википедия Оксид золота(III) — Общие … Википедия Оксид золота(I) — Общие Систематическое наименование Оксид золота(I) Традиционные названия Закись золота, окись золота Химическая формула Au2O Физические свойства Сост … Википедия Оксид марганца(IV) — Общие … Википедия Оксид хрома(VI) — Общие … Википедия Оксид золота(I,III) — Общие Систематическое наименование Оксид золота(I,III) Традиционные названия Окисел золота; аурат золота Химическая формула Au[AuO2] Рациональная формула AuO … Википедия Оксид меди(I) — Оксид меди(I) … Википедия Оксид платины(II) — Общие Систематическое наименование Оксид платины(II) Традиционные названия Окисел платины Химическая формула PtO Физические свойства Состояние ( … Википедия Оксид платины(III) — Общие Систематическое наименование Оксид платины(III) Традиционные названия Окисел платины Химическая формула Pt2O3 Физические свойства … Википедия Оксид калия, характеристика, свойства и получение, химические реакцииОксид калия, характеристика, свойства и получение, химические реакции.Оксид калия – неорганическое вещество, имеет химическую формулу K2O. Краткая характеристика оксида калия:Оксид калия – неорганическое вещество бесцветного либо бледно-желтого цвета. Так как валентность калия равна одному, то оксид калия содержит один атом кислорода и два атома калия. Химическая формула оксида калия K2O. В воде не растворяется, а вступает в реакцию с ней. Растворим в органических растворителях. Обладает высокой гигроскопичностью. Физические свойства оксида калия:
калия окись (рус.) | ||||||
| Тип вещества | неорганическое | |||||
| Внешний вид | бесцветные (иногда бледно-желтый) кубические кристаллы | |||||
| Цвет | бесцветный, иногда – бледно-желтый | |||||
| Вкус | —* | |||||
| Запах | — | |||||
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество | |||||
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м 3 | 2320 | |||||
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см 3 | 2,32 | |||||
| Температура кипения, °C | — | |||||
| Температура плавления, °C | 740 | |||||
| Температура разложения, °C | 300 | |||||
| Гигроскопичность | высокая гигроскопичность | |||||
| Молярная масса, г/моль | 94,196 |
Получение оксида калия:
Оксид калия получается в результате следующих химических реакций:
Вначале получают пероксид калия.
Затем пероксид калия обогащают калием.
Напрямую оксид калия путем окисления самого калия не получается.
Химические свойства оксида калия. Химические реакции оксида калия:
Химически активное вещество.
1. реакция оксида калия с галогенами:
Оксид калия бурно реагирует с галогенами, образуя соответственно две соли:
– хлорид калия и гипохлорит калия,
– бромид калия и гипобромит калия,
– йодид калия и гипойодит калия.
2. реакция оксида калия с водой:
3. реакция оксида калия с оксидом углерода (углекислым газом):
Оксид калия на воздухе реагирует с углекислым газом (являющийся кислотным оксидом), образуя соль – карбонат калия.
4. реакция оксида калия с оксидом серы:
Оксид серы также является кислотным оксидом. В результате реакции образуется соответственно соль – в первом случае – сульфит калия, во втором случае – сульфат калия.
5. реакция оксида калия с оксидом кремния:
Оксид кремния также является кислотным оксидом. В результате реакции образуется соль – силикат калия.
Аналогично проходят реакции оксида калия и с другими кислотными оксидами.
6. реакция оксида калия с оксидом цинка :
Оксид цинка является амфотерным оксидом. Это значит, что как амфотерный оксид оксид цинка проявляет свойства как кислотных, так и основных соединений. В результате реакции образуется соль – цинкат калия.
Аналогично проходят реакции оксида калия и с другими амфотерными оксидами.
7. реакция оксида калия с плавиковой кислотой:
В результате химической реакции получается соль – фторид калия и вода.
Аналогично проходят реакции оксида калия и с другими кислотами.
8. реакция оксида калия с бромистым водородом (бромоводородом):
9. реакция оксида калия с йодоводородом:
10. реакция оксида калия с жидким аммиаком:
В результате химической реакции получается гидроксид калия и амид калия.
Применение и использование оксида калия:
Примечание: © Фото //www.pexels.com, //pixabay.com
оксид калия реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие оксида калия
реакции с оксидом калия
Мировая экономика
Справочники
Востребованные технологии
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Формула оксида калия (K2O), свойства, риски и использование
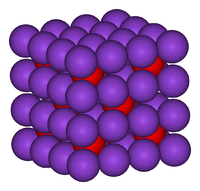
оксид калия, также называется оксидом калия, ионная кислородно-калиевая соль, формула которой K2О. Его структура представлена на рисунке 1 (EMBL-EBI, 2016).
К2Или это самый простой оксид калия, это очень реактивное и редко встречающееся соединение. Некоторые коммерческие материалы, такие как удобрения и цементы, испытывают, предполагая процентное содержание состава, которое будет эквивалентно смеси химических соединений K2О.
Оксид калия получают из гидроксида калия (едкого кали) и металлического калия при 450 ° C с образованием молекулярного водорода (ОКСИД КАЛИЯ K2O, S.F.) в соответствии с уравнением:
Его также получают путем восстановления пероксида калия в соответствии с реакцией:
Другим способом получения оксида калия является нагревание карбоната калия при высокой температуре, как показано следующей реакцией:
Однако основным способом получения оксида калия является нагревание нитрата калия для получения молекулярного азота, как показано следующей реакцией:
Физико-химические свойства
Соединение имеет молекулярную массу 94,2 г / моль и плотность 2,13 г / мл при 24 ° С. Он имеет температуру плавления 740 ° C, хотя начинает разлагаться при 300 ° C (Royal Society of Chemistry, 2015).
Соединение устойчиво к нагреванию и растворим в этаноле и эфире. К2Или он кристаллизуется в структуре антифторита. По этой причине положения анионов и катионов меняются местами относительно их положений в CaF.2, с ионами калия, координированными до 4 оксидных ионов, и ионами оксида, скоординированными с 8 калиями.
К2Или это основной оксид и бурно реагирует с водой с образованием едкого гидроксида калия. Он распух и поглощает воду из атмосферы, инициируя эту энергичную реакцию.
Оксид калия обратимо окисляется до пероксида калия при 350 ° С, бурно реагирует с кислотами, такими как соляная кислота, с образованием солей калия в соответствии с реакцией:
Соединение реагирует с диоксидом азота с образованием нитрата и нитрита калия при температуре от 150 до 200 ° C:
Оксид калия реагирует при низких температурах с аммиаком с образованием амидов и гидроксида калия в соответствии с реакцией:
Реактивность и опасности
Оксид калия является нестабильным веществом. Он легко окисляется до других оксидов калия, пероксида или до окиси калия (KHO). Соединение не является горючим, но активно и экзотермически реагирует с водой с образованием гидроксида калия (KOH).
Раствор оксида калия в воде является сильным основанием, бурно реагирует с кислотой и вызывает коррозию. Бурно реагирует с водой, образующей гидроксид калия. Атакует многие металлы в присутствии воды (Национальный институт безопасности и гигиены труда, 2014).
Вещество разъедает глаза, кожу и дыхательные пути, а также при попадании в организм. Вдыхание аэрозоля может вызвать отек легких. Симптомы отека легких часто проявляются лишь через несколько часов и усиливаются при физической нагрузке..
В случае попадания в глаза вам следует проверить, носите ли вы контактные линзы, и немедленно снять их. Глаза должны быть промыты проточной водой в течение не менее 15 минут с открытыми веками. Вы можете использовать холодную воду. Мазь не следует использовать для глаз.
Если химическое вещество попало на одежду, удалите его как можно быстрее, защищая свои руки и тело. Поместите жертву под безопасный душ.
Если химическое вещество накапливается на незащищенной коже жертвы, например на руках, аккуратно и осторожно промойте кожу, загрязненную проточной водой и неабразивным мылом. Вы можете использовать холодную воду. Если раздражение не проходит, обратитесь к врачу. Выстирать загрязненную одежду перед повторным использованием.
Если контакт с кожей серьезный, его следует промыть дезинфицирующим мылом и покрыть кожу, загрязненную антибактериальным кремом..
В случае вдыхания пострадавшему должно быть разрешено отдыхать в хорошо проветриваемом помещении. Если вдыхание серьезное, пострадавшего следует как можно скорее эвакуировать в безопасное место..
Ослабьте тесную одежду, такую как воротник рубашки, ремни или галстук. Если пострадавшему трудно дышать, следует назначить кислород. Если пострадавший не дышит, проводится реанимация из уст в уста.
Всегда принимая во внимание, что человеку, оказывающему помощь в проведении реанимации изо рта в рот, может быть опасно, когда вдыхаемый материал токсичен, инфекционен или вызывает коррозию.
В случае проглатывания не вызывать рвоту. Ослабьте тесную одежду, такую как воротники рубашки, ремни или галстуки. Если пострадавший не дышит, проведите реанимацию из уст в уста. Во всех случаях следует немедленно обратиться за медицинской помощью (IPCS, S.F.).
приложений
Химическая формула К2O (или просто «K») используется в нескольких промышленных контекстах: числа N-P-K для удобрений, в формулах цемента и в формулах стекла.
Оксид калия часто не используется непосредственно в этих продуктах, но количество калия указывается в терминах K-эквивалентов.2Или для любого типа используемых соединений калия, таких как карбонат калия.
Поэтому, если удобрением является хлорид калия в количестве 30% по весу, его стандартный индекс калия, основанный на оксиде калия, будет составлять только 18,8%. Он производится и / или импортируется от 10 до 100 тонн в год этого вещества в Европейском экономическом пространстве.
Это вещество используется в лабораторных химикатах, удобрениях, полимерах и фитосанитарных продуктах. К2Или это имеет промышленное использование, которое приводит к производству другого вещества (использование промежуточных продуктов).
Оксид калия используется в областях приготовления смесей и / или переупаковки, а также в сельском хозяйстве, лесном хозяйстве и рыболовстве. Это вещество используется для производства химических продуктов, пластмассовых изделий и минеральных продуктов (например, гипса, цемента)..
Выброс в окружающую среду оксида калия, вероятно, произойдет для промышленного использования: в качестве промежуточного этапа при производстве другого вещества (использование промежуточных продуктов), составления смесей, в качестве вспомогательного средства для обработки и промышленной обработки на истирание с низкой скоростью. выпуска, резки, механической обработки или полировки металла).
Возможно, что другое высвобождение в окружающую среду этого вещества путем его использования во внутренних помещениях, например, моющих жидкостей / моющих средств, автомобильных средств по уходу, краски и покрытия или клеи, ароматизаторы и освежители воздуха..
Также для использования внутри помещений в закрытых системах с минимальным выбросом, таких как охлаждающие жидкости в холодильниках, электрические нагреватели на масляной основе.
Оксид калия используется на открытом воздухе в долговременных материалах с низкой скоростью высвобождения, например, в строительных материалах и конструкциях из металла, дерева и пластика..
В помещении он используется в долговечных материалах с низкой скоростью высвобождения, таких как мебель, игрушки, строительные материалы, занавески, обувь, кожгалантерея, бумажные и картонные изделия, электронное оборудование..
Это вещество можно найти в изделиях из камня, гипса, цемента, стекла или керамики (например, посуду, кастрюли / сковородки, контейнеры для хранения продуктов питания, строительные и изоляционные материалы) (Европейское химическое агентство, 2017).
Оксид калия является термостойким, крайне нерастворимым источником калия, подходящим для стекла, оптики и керамики. Оксидные соединения не приводят к электричеству.
Однако некоторые структурированные оксиды перовскита являются электронными проводниками, которые находят применение в катоде твердооксидных топливных элементов и системах генерации кислорода..
Они представляют собой соединения, которые содержат, по меньшей мере, один кислородный анион и один катион металла. Они чрезвычайно стабильны, что делает их полезными для изготовления керамических конструкций, таких как глиняные миски или для продвинутой электроники.
Он также используется в легких конструкционных компонентах в аэрокосмической и электрохимической промышленности, таких как топливные элементы, в которых они проявляют ионную проводимость..
Металлооксидные соединения являются основными ангидридами и поэтому могут вступать в реакцию с кислотами и сильными восстановителями в окислительно-восстановительных реакциях..
Оксид калия
Оксид калия – соединение калия с кислородом. Химическая формула – K2O. Является компонентом всех калийных и калийсодержащих удобрений.
Традиционно содержание Калия в удобрениях выражают содержанием Оксида калия. Все свойства Калия, как питательного элемента описаны в статье Калий.
Химические и физические свойства
Оксид калия – твердое кристаллическое вещество, образующее бесцветные кристаллы. Имеет две устойчивые кристаллические модификации: кубическую (до 372°С) и гексагональную (выше 372°С).
Оксид калия на воздухе расплавляется и, поглощая CO2, дает K2CO3. Бурно взаимодействует с водой с образованием КОН. Реагирует с эфиром и спиртом.
При температуре 250°С вступает в реакцию с H2. При этом образуются КОН. При этой же температуре взаимодействует с NH3, образуя КОН и KNH2.
Трехмерная модель молекулы
Энергично вступает в реакции взаимодействия с галогенами, расплавленной серой, различными кислотами. При нагревании с оксидами бора, алюминия, кремния образует соответственно бораты, алюминаты и полисиликаты.
При нагревании с NO2 образуется смесь KNO3 и KNO2.
Оксид калия получают:
Содержание оксида калия в почве и удобрениях
Доступность калия для растений зависит от формы доступности калия в почве. Катионы ППК и водорастворимые соединения калия являются основными источниками калийного питания растений. В этой связи степень обеспеченности почвы калием для нужд питания растений выражают содержанием в подвижной форме и через оксид калия K2O. Эта величина обозначает суммарное количество обменного и водорастворимого кальция в мг/кг почвы. [1]
Удобрения содержат различное количество оксида калия. Например, хлористый калий включает в себя 57–60 % калия в пересчете на K2O. Фиксированный почвой калий из удобрений доступен для растений. При этом степень его доступности тем выше, чем больше его фиксировано почвой. [2]
Калийные удобрения отличаются высокой растворимостью в воде. При внесении в почву они быстро растворяются и на основании обменных реакций вступают во взаимодействие с ППК. Часть калия удобрений переходит в необменные фиксированные почвенные соединения. [2]

















