что такое сложные белки
Сложные белки
Сло́жные белки́ (протеиды, холопротеины) — двухкомпонентные белки, в которых помимо пептидных цепей (простого белка) содержится компонент неаминокислотной природы — простетическая группа. При гидролизе сложных белков, кроме свободных аминокислот, освобождается небелковая часть или продукты её распада.
В качестве простетической группы могут выступать различные органические (липиды, углеводы) и неорганические (металлы) вещества.
Среди сложных белков выделяют следующие основные классы: гликопротеины, липопротеины, хромопротеины, нуклеопротеины, фосфопротеины и металлопротеины.
Смотреть что такое «Сложные белки» в других словарях:
сложные белки — (холопротеины) – белки, содержащие компонент небелковой природы – простетическую группу … Краткий словарь биохимических терминов
сложные белки — протеиды … Cловарь химических синонимов I
белки — 1. БЕЛКИ, ов; мн. (ед. белок, лка; м.). 1. Выпуклые непрозрачные оболочки глаз белого цвета. Б. у неё голубоватые. 2. Разг. сниж. О глазах. Вращать белками. ◁ Белочный, ая, ое. Б ые оболочки глаз. 2. БЕЛКИ, ов; мн. (ед. белок, лка; м.). Сложные… … Энциклопедический словарь
БЕЛКИ — природные высокомолекулярные органические соединения, построенные из остатков 20 аминокислот, которые соединены пептидными связями в длинные цепи. Молекулярная масса от нескольких тысяч до нескольких миллионов. В зависимости от формы белковой… … Большой Энциклопедический словарь
Белки — У этого термина существуют и другие значения, см. Белки (значения). Белки (протеины, полипептиды[1]) высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью альфа аминокислот. В живых организмах… … Википедия
БЕЛКИ — (протеины), класс сложных азотсодержащих соединений, наиболее характерных и важных (наряду с нуклеиновыми кислотами) компонентов живого вещества. Белки выполняют многочисленные и разнообразные функции. Большинство белков ферменты, катализирующие… … Энциклопедия Кольера
Белки — I Белки (протеины) органические соединения, структурной основой которых служит полипептидная цепь, состоящая из аминокислотных остатков, соединенных пептидными связями ( СО NH2 ) в определенной последовательности. Белки являются главными… … Медицинская энциклопедия
БЕЛКИ (органические соединения) — БЕЛКИ, высокомолекулярные органические соединения, биополимеры, построенные из 20 видов L a аминокислотных остатков, соединенных в определенной последовательности в длинные цепи. Молекулярная масса белков варьируется от 5 тыс. до 1 млн. Название… … Энциклопедический словарь
БЕЛКИ — БЕЛКИ, или протеины, высокомолекулярные коллоидальные органические вещества, построенные из остатков аминокислот. Б. по своему количественному содержанию в организме животных занимают среди твердых составных частей его одно из первых мест, а по… … Большая медицинская энциклопедия
БЕЛКИ — (Sciurus), род беличьих. Дл. тела 20 31 см. Хорошо лазают и передвигаются по деревьям. Длинный (20 30 см) пышный хвост служит рулём при прыжках. Ок. 40 видов, в Сев. полушарии и на С. Юж. Америки, в горных и равнинных лесах, включая островные… … Биологический энциклопедический словарь
Сложные белки
В качестве простетической группы могут выступать различные органические (липиды, углеводы) и неорганические (металлы) вещества.
В зависимости от химической природы простетических групп среди сложных белков выделяют следующие классы:
* Гликопротеиды, содержащие в качестве простетической группы ковалентно связанные углеводные остатки и их подкласс — протеогликаны, с мукополисахаридными простетическими группами. В образовании связи с углеводными остатками обычно участвуют гидроксильные группы серина или треонина. Большая часть внеклеточных белков, в частности, иммуноглобулины — гликопротеиды. В протеогликанах углеводная часть составляет
95 %, они являются основным компонентом межклеточного матрикса.
* Липопротеиды, содержащие в качестве простетической части нековалентно связанные липиды. Липопротеиды, образованные белками-аполипопротеинами связывающимися с ними липидами и выполняют функцию транспорта липидов.
* Металлопротеины, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеидов есть белки, выполняющие депонирующие и транспортные функции (например, железосодержащие ферритин и трансферрин) и ферменты (например, цинксодержащая карбоангидраза и различные супероксиддисмутазы, содержащие в качестве активных центров ионы меди, марганца, железа и других металлов)
Нуклеопротеины, содержащие нековалентно связанные ДНК или РНК, в частности, хроматин, из которого состоят хромосомы, является нуклеопротеидом.
Фосфопротеиды, содержащие в качестве простетической группы ковалентно связанные остатки фосфорной кислоты. В образовании сложноэфирной связи с фосфатом участвуют гидроксильные группы серина или треонина, фосфопротеинами являются, в частности, казеин молока:
* Хромопротеиды — собирательное название сложных белков с окрашенными простетическими группами различной химической природы. К ним относится множество белков с металлосодержащей порфириновой простетической группой, выполняющие разнообразные функции — гемопротеины (белки, содержащие в качестве простетической группы гем — гемоглобин, цитохромы и др.), хлорофиллы; флавопротеиды с флавиновой группой, и др.
Связанные понятия
Метаболи́зм (от греч. «превращение», «изменение») или обме́н веще́ств — набор химических реакций, которые возникают в живом организме для поддержания жизни. Эти процессы позволяют организмам расти и размножаться, сохранять свои структуры и отвечать на воздействия окружающей среды.
Упоминания в литературе
Связанные понятия (продолжение)
Тетрáсахариды (от др. греч. τέσσερις — четыре — два и ζάχαροη — сахар) — органические соединения, одна из групп углеводов; являются частным случаем олигосахаридов.
Фитазы (мио-инозитол-1,2,3,4,5,6-гексакисфосфат-фосфогидролазы) – группа ферментов, относящихся к подклассу фосфатаз, осуществляющих высвобождение хотя бы одного фосфат-иона из молекулы фитиновой кислоты. В результате гидролиза фитиновой кислоты образуются низшие, т. е. содержащие менее шести остатков фосфорной кислоты, инозитолфосфаты, инозитол и неорганический фосфат, а также высвобождаются связанные с фитатами катионы.
Хромопротеиды (от греч. chroma — краска) — сложные белки, состоящие из простого белка и связанного с ним окрашенного небелкового компонента — простетической группы. Различают гемопротеины (содержат в качестве простетической группы гем), магнийпорфирины и флавопротеины (содержат производные изоаллоксазина). Хромопротеиды участвуют в таких процессах жизнедеятельности, как фотосинтез, клеточное дыхание и дыхание всего организма, транспорт кислорода и углекислого газа, окислительно-восстановительные.
Сложные белки



Это структуры, содержащие белковую часть – апопротеин и небелковый компонент – простетическую группу. В зависимости от строения последней принято различать следующие их варианты.
Фосфопротеины – это сложные белки, простетической группой которых является остаток фосфорной кислоты. Тип связи между апопротеином и небелковым компонентом – сложноэфирная, которая образуется при взаимодействии ОН-группы серина или треонина с фосфорной кислотой. К протеинам этого класса относятся казеиноген молока, фосфорилированные модификации гистонов, ферменты (РНК-полимеразы, некоторые фосфотрансферазы, фосфатазы) и другие, а также вителлин, фосвитин желтка и овальбумин белка яиц, ихтуллин икры рыб.
Остатки фосфорной кислоты, включённые в белки, находятся в диссоциированом состоянии, что придаёт молекуле сильный отрицательный заряд. Поэтому фосфопротеины могут легко взаимодействовать с лигандами или отталкивать их. Так, например, они связывают ионы Са 2+ и транспортируют их.
Но главная особенность данной простетической группы – это возможность изменения конформации и заряда белковой молекулы, что сказывается на её свойствах и функциях. Реакция взаимодействия с фосфорной кислотой называется фосфорилирование или дефосфорилирование и используется, например, для регулирования активности ферментов и изменения функциональной активности биомембран (проницаемости и др.).
Фосфопротеины необходимы для развития зародыша, плода, новорожденного, т.к. содержат оптимальный набор аминокислот, а фосфорная кислота используется для формирования скелета (связывание ионов Са 2+ ), для образования макроэргов – АТФ, АДФ и др., которые требуются в качестве источников энергии в реакциях синтеза, особенно интенсивно протекающих в растущем организме.
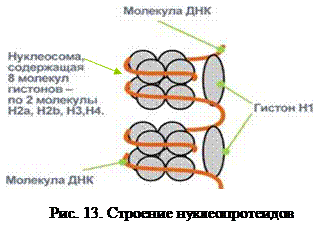
Нуклеопротеины – сложные белки, простетической группой которых являются нуклеотиды, и в первую очередь нуклеиновые кислоты – ДНК и РНК. В качестве апопротеина выступают белки гистоны, реже протамины. Так как эти протеины положительно заряжены, а нуклеиновые кислоты – отрицательно, то связь, образуемая между ними, ионная. Множество октамеров гистонов, комплексируясь с полинуклеотидом, образует нуклеосомы, которые затем компактно укладываются в органоидах (рис. 13).
В функциональном отношении они отвечают за хранение и передачу наследственной информации и процессы биосинтеза белка.
Хромопротеины («цветные белки») своей окраской обязаны простетической группе – пигменту. В зависимости от строения различают следующие подклассы: гемопротеины, флавопротеины, родопсин.
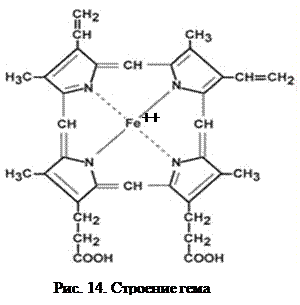
Миоглобин – небольшой глобулярный белок (Mr 16500 Да); молекула его состоит из одной полипептидной цепи (153 а/к) и одного гема. Сродство к кислороду у данного гемопротеида значительно больше, чем у гемоглобина, поэтому он может принимать газ от последнего для сохранения или использования его в мышечных клетках.
Гем b является также структурной единицей ферментов каталазы и пероксидазы, обезвреживающих пероксиды, и цитохромов – митохондриальных белков, участвующих в переносе электронов от окисляемых веществ в конечном итоге на кислород за счёт своей способности изменять валентность железа.
Гем а встречается в растительных гемопротеинах и участвует в процессе фотосинтеза.
Металлопротеины – сложные белки, где роль небелкового компонента выполняют катионы металлов. Связь между ними ионная или координационная (донорно-акцепторная). Типичными представителями таких белков являются железосодержащие белки.
Ферритин. В его составе ионы Fe 3+ депонируются в клетках селезёнки, костного мозга, но богаче всего этим белком печень. Там может накапливаться до 700 мг железа, которое используется по мере надобности для синтеза гема. Гемосидерин – это комплекс гликопротеина и ионов железа, образуется в тканях при кумулировании избытка железа. Трансферрин – растворимый в воде железопротеин, содержащий ещё олигосахариды (металлогликопротеин). Этот белок вырабатывается гепатоцитами и секретируется в кровь, где служит для транспорта катионов этого металла к клеткам других органов. Молекула трансферрина удерживает два иона железа, которые захватывает в кишечнике или местах распада гема, и осуществляет их перенос к точкам депонирования и утилизации. Церулоплазминаналогично трансферрину обеспечивает транспорт катионов металла, только восьми ионов меди.
Гликопротеины,или гликоконъюгаты. В них простетическая группа представлена углеводными компонентами и связана с белком О-гликозидными (реже N-гликозидными) связями. Небелковый фрагмент некоторых гликопротеидов редко бывает представлен одним моносахаридом; как правило, это олиго- или полисахаридные разветвлённые цепочки. Причём на долю углеводов может приходиться от 1 до 85%.
Исходя из вклада в общую копилку, выделяют два подкласса белков, содержащих углеводы: протеогликаныи гликопротеины. Между ними имеются существенные отличия:
Белки и пептиды. Структуры и функции. Сложные белки
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Белки и пептиды. Структуры и функции. Сложные белки
Белки — высокомолекулярные природные полимеры, состоящие из аминокислотных остатков, соединенных пептидной связью; являются главной составной частью живых организмов и молекулярной основой процессов жизнедеятельности.
БЕЛКИ. КЛАССИФИКАЦИЯ БЕЛКОВ
I. Функциональная (по функции, выполняемой в организме)
II. По форме молекулы
III. По степени сложности молекулы
БЕЛКИ. ФУНКЦИИ ПЕПТИДОВ
Протеиногенные аминокилоты являются альфа-аминокислотами (кроме пролина).
БЕЛКИ. КЛАССИФИКАЦИЯ аминокислот
I. По строению радикала
II. По кислотно-основным свойствам
III. По полярности
а) незаряженные (сер, тре, цис, гли, тир,асн, глн);
Нестандартные аминокилоты в составе белков:
БЕЛКИ. СВОЙСТВА АМИНОКИСЛОТ
Кислотно-основные свойства
Аминокислоты имеют 2 функциональные группы с противоположными свойствами: кислую карбоксильную и основную аминогруппу. Поэтому в водном растворе аминокислоты существуют в виде биполярного иона.
Нейтральные аминокислоты в воде не имеют заряда. Дикарбоновые аминокислоты имеют две карбоксильные группы, которые диссоциируют, отдавая 2 протона, но поскольку у них только одна аминогруппа, принимающая один протон, то такие аминокислоты ведут себя как кислоты и раствор их имеет кислую реакцию. Сам ион аминокислоты заряжается отрицательно.
Диаминомонокарбоновые аминокислоты реагируют в водном растворе как слабые основания, так как один протон, который освобождается при диссоциации карбоксильной группы таких аминокислот, связывается с одной из аминогрупп, а вторая аминогруппа связывает протон из водного окружения, в результате увеличивается количество OH – групп и повышается pH. Заряд иона таких аминокислот будет положительным.
Добавляя к раствору аминокислоты определенное количество кислоты или щелочи, можно изменить их заряд. При определенном значении pH наступает такое состояние, при котором заряд аминокислоты становится нейтральным. Такое значение pH получило название изоэлектрической точки (ИЭТ). При значении pH, равном изоэлектрической точке, аминокислоты не перемещаются в электрическом поле. Если pH ниже изоэлектрической точки, катион аминокислоты движется к катоду, а при pH выше ИЭТ анион аминокислоты — к аноду. На этих свойствах аминокислот основана возможность разделения их в электрическом поле (электрофорез). Кислые аминокислоты имеют ИЭТ в слабокислой среде, основные — в слабоосновной, а нейтральные — в нейтральной.
Обусловлена наличием у аминокислоты ассиметричного атома углерода (называется хиральный центр).
АК могут быть L- или D-стереоизомеры. В состав белков организма входят L-стереоизомеры аминокислот.
Все аминокислоты поглощают свет в инфракрасной области спектра. Три циклических аминокислоты (фенилаланин, тирозин и триптофан) поглощают свет в ультрафиолетовой области при
280 нм.
УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКОВЫХ МОЛЕКУЛ
Первичная структура — это конфигурация полипептидной цепи, которая формируется в результате образования пептидной связи между остатками АК.
Постулаты (принципы формирования пептидной связи), сформулированные Л. Поллингом и Р. Кори:
1) атомы, образующие пептидную связь, копланарны (расположены в одной плоскости); вращение атомов или групп атомов вокруг пептидной связи невозможно;
2) принцип эквивалентности вклада АК-остатков в образование пептидной связи и, тем самым, в образование полипептидной цепи (исключение пролин);
3) принцип максимума водородных связей.
Первичную структуру белка стабилизируют (поддерживают):
Первичная структура белка несет информацию о его пространственной структуре.
Вторичная структура белка — локальная конформация, обусловленная вращением отдельных участков полипептидной цепи вокруг одинарных ковалентных связей.
Основные связи, которые стабилизируют вторичную структуру, — водородные.
Виды вторичной структуры:
Несколько участков полипептидной цепи, организованных в пространстве в форме альфа-спирали или бета-структуры, могут объединяться, формируя надвторичную структуру. В результате в молекуле белка образуются домены (функциональные или структурные).
Третичная структура белка — это расположение в пространстве всей полипептидной цепи, отдельные участки которой имеют собственную локальную конформацию.
Этапы формирования третичной структуры (см. рис.):
Поддержанию третичной структуры белка способствуют гидрофобные связи, которые образуются внутри молекулы. В образовании этих связей принимают участие неполярные радикалы аминокислот. Могут также образовываться другие нековалентные связи.
У белка, имеющего третичную структуру, на поверхности молекулы формируется участок, который может присоединять к себе другие молекулы, называемые лигандами. Этот участок называется активный центр и формируется из радикалов аминокислот, которые сближаются друг с другом при формировании третичной структуры. Высокая специфичность взаимодействия белка с лигандом обеспечивается комплементарностью структуры активного центра структуре лиганда.
Четвертичная структура формируется при объединении нескольких полипептидных цепей, имеющих третичную структуру. Образованный таким образом белок обладает новой функцией.

Белки с четвертичной структурой называются олигомерными, а составляющие их индивидуальные полипептидные цепи — протомерами или мономерами. Такие соединения стабилизируются водородными связями и электростатическими взаимодействиями между АК-остатками, расположенными на поверхности протомеров.
Преимущества белков с четвертичной структурой:
1) экономия генетического материала;
2) уменьшение числа ошибок при синтезе белка;
3) качественное разнообразие белков — появление у белков новых функций.
Сложные белки
Многие белки в своем составе, помимо аминокислот, могут содержать и небелковые компоненты. Эти соединения в составе белков называют простетической группой. Простетические группы с белком соединяются разными типами связей.
В зависимости от химического состава простетической группы сложные белки можно разделить на несколько классов.
1. Хромопротеины. Это белки, простетическая группа которых имеет окраску. К ним относятся многие белки, содержащие металлы. Например, церулоплазмин — белок, содержащий медь, имеет синюю окраску. Белки, содержащие железо: гемоглобин, миоглобин, цитохромы. Они имеют красную окраску. Присутствие витамина B2 придает белкам желтый цвет (флавопротеины).
Простетическая группа хромопротеинов связана с гистидином полипептидной цепи координационными связями.
2. Гликопротеины. Это белки, простетическая группа которых содержит углеводы. Углевод соединяется с белковой частью ковалентными связями. В соединении с углеводом участвует OH-группа аминокислоты серина или треонина. Гликопротеины — это часть белково-углеводных комплексов. Этим белкам принадлежит важная роль в структурной организации клеток и тканей, они выполняют защитные функции. Основная часть внеклеточных белков — это гликопротеины.
3. Липопротеины. Это белки, простетическая группа которых содержит липиды. Они обеспечивают транспорт липидов в крови, являются компонентами биологических мембран. Связи между белковой частью молекулы и липидом — гидрофобные или ионные.
4. Металлопротеины. Это белки, простетическая группа которых представлена металлами. Они транспортируют или участвуют в депонировании металлов (ферритин, трансферрин). Между белком и простетической группой образуются координационные связи.
5. Нуклеопротеины. Простетическая группа у таких белков — нуклеиновая кислота. Различают дезоксирибонуклеопротеины (простетическая группа — ДНК) и рибонуклеопротеины (простетичесая группа — РНК). Им принадлежит важная роль в хранении, передаче и реализации генетической информации. Между белком и молекулой нуклеиновой кислоты образуются ионные связи.
6. Фосфопротеины. Белки, которые содержат в своем составе фосфорную кислоту. Используются для регуляции процессов жизнедеятельности (фосфорилирование / дефосфорилирование). Между белком и остатком фосфорной кислоты формируются сложноэфирные связи, в образовании которых участвует OH-группа серина.
БЕЛКИ соединительных тканей
(Молекулы внеклеточного матрикса)
Главный компонент внеклеточного матрикса — белки. Выделяют 3 группы белков:
Все эти белки содержат углеводы, поэтому относятся к сложным белкам и называются белково-углеводные комплексы (БУК).
БУК классифицируются по 2 критериям: количеству углеводов в комплексе и качественному углеводному составу:
ПГ — это белковые комплексы, в которых с молекулами белка ковалентно связаны гликозаминогликаны (ГАГ). Белки ПГ называют коровыми белками (core — сердцевина, стержень).
ГАГ — гетерополисахариды, построенные по стандартному принципу: состоят из многократно повторяющихся дисахаридов, мономерами которых являются уроновые кислоты и гексозамины. Классифицируют ГАГ по строению остатков моносахаридов, типу связи между ними, числу и локализации сульфатных групп. Выделяют несколько семейств ГАГ:
Строение главного ПГ хрящевой ткани — агрекана:
Функции ПГ: 1) структурные компоненты внеклеточного матрикса; 2) специфически взаимодействуют с коллагеном, эластином, фибронектином, ламинином и другими белками матрикса; 3) как полианионы, они связывают поликатионы и катионы; 4) обеспечивают тургор (упругость) различных тканей, связывая воду; 5) противостоят компрессионным силами; 6) влияют на клеточную миграцию; 7) действуют как антикоагулянты.
Гликопротеины и мукопротеины часто считают синонимами, так как различия между ними касаются лишь количества углеводов в комплексе, а моносахариды глико- и мукопротеинов одинаковы: галактоза, манноза, гексозамины, нейраминовая и сиаловая кислоты.
Функции мукопротеинов: 1) как компоненты секретов слизистых оболочек, они обладают защитными свойствами, уменьшая трение соприкасающихся поверхностей; 2) обеспечивают групповую, видовую и тканевую специфичность; 3) обладают ферментативной активностью.
Функции гликопротеинов: 1) являются структурными компонентами мембраны клетки, коллагеновых, эластиновых и фибриновых волокон, костного матрикса; 2) транспортные молекулы для витаминов, липидов, микроэлементов; 3) обеспечивают иммунную защиту; 4) обладают гормональной и ферментативной активностью (тиротропин, факторы свертывания крови).
В зависимости от типа связи между углеводной и белковой частями БУК различают 2 типа БУК:
Белковые части обоих типов БУК синтезируются по законам матричного синтеза, а углеводные части — нематрично по двум механизмам:
Распад БУК катализируется с помощью ферментов лизосом. Белковую часть расщепляют протеиназы, а углеводную цепь — гликозидазы. При врожденных дефектах гликозидаз возникают заболевания — мукополисахаридозы (болезни накопления БУК, лизосомные болезни).
Фибриллярные структурные белки
Коллагены — основные гликопротеины соединительных тканей. Они составляют 25% всех белков организма человека и обеспечивают сопротивление растяжению в отличие от ПГ, которые противодействуют сжатию. В геноме человека 30 генов, кодирующих коллагеновые α-цепи. Выделено свыше 20 типов коллагеновых молекул (изоколлагены).
| Тип коллагена | Длина волокна | Состав | Выделен из |
| Тип I | 300 нм | [α(I)]2α2(I) | Кости, роговицы, дентина, клапанов сердца, стенки матки |
| Тип II | 300 нм | [α(II)]3 | Гиалинового хряща, стекловидного тела |
| Тип III | 300 нм | [α(III)]3 | Дермы, клапанов сердца, десны |
| Тип IV | 390 нм | [α(IV)]3 | Базальных мембран |
| Тип V | 300 нм | [α(V)]2α2(V) | Кости, роговицы, больших сосудов, клапанов сердца |
| Тип VI | 105 нм | α1(VI), α2(VI) | Кровеносных сосудов |
| Тип VII | 450 нм | α1(VII) | Эндотелия сосудов |
| Тип VIII | 150 нм | α1(VIII) | Эндотелия сосудов |
| Тип IX | 200 нм | α1(IX) α2(IX) | Хрящевой ткани |
| Тип X | 150 нм | α1(X) | Хрящевой ткани |
Изоколлагены типов I–III получили название фибрилформирующих коллагенов, а изоколлагены IX и XII — фибриллассоциируемых коллагенов, так как они обычно связаны с коллагеновыми волокнами, которые образовали фибрилформирующие коллагены. Фибриллассоциируемые коллагены обеспечивают соединение волокон с другими молекулами матрикса. Типы IV и VII называют сетьформирующими коллагенами. Они образуют сетевидные структуры и чаще всего находятся в базальных мембранах, обеспечивая связь клеточных слоев эпителия с подлежащей соединительной тканью. Это особенно важно для кожи.
Первичная структура коллагена — одиночная полипептидная цепь:
1/3 – ГЛИ, 1/5 – ПРО и гидроксиПРО (ОН-ПРО), есть и ОН-ЛИЗ. К ней присоединен дисахарид (глюкоза + галактоза). Полипептидная цепь — левозакрученная спираль, но водородные связи отсутствуют, так как много иминокислот.
Вторичная структура — особый коллагеновый тип: 3 полипептидные цепи сворачиваются в тройную спираль. Эта спираль — правозакрученная.
Синтез коллагена. Полипептидные цепи синтезируются на полисомах в виде препроколлагена («пре» указывает на наличие сигнального, лидирующего пептида; «про» — на наличие дополнительных пептидов на N- и С-концах). Затем начинается процессинг препроколлагена.
| Порядок и локализация процессинга препроколлагена | |
| Внутриклеточно | Внеклеточно |
| 1. Удаление сигнального пептида 2. Гидроксилирование ПРО и ЛИЗ 3. Гликозилирование ОН-ЛИЗ 4. Образование внутри- и межцепочечных S-S связей в дополнительных пептидах 5. Образование тройной спирали | 1. Удаление дополнительных пептидов 2. Образование коллагеновых волокон с поперечной исчерченностью 3. Окислительное дезаминирование ε-аминогрупп ЛИЗ и ОН-ЛИЗ с образованием альдегидных групп 4. Образование поперечных связей в коллагеновых волокнах |
Разрушается коллаген коллагеназами и лизосомными ферментами — протеиназами и гликозидазами. О «возрасте» коллагена можно судить по количеству поперечных ковалентных связей в коллагеновых волокнах: чем «моложе» коллаген, тем меньше поперечных связей, тем легче и быстрее он разрушается, и наоборот.
Эластин. Молекула эластина состоит из двух типов фрагментов, чередующихся вдоль цепи: гидрофобные (фибриллярные) сегменты, которые ответственны за эластические свойства молекулы и глобулярные сегменты, богатые АЛА и ЛИЗ, имеющие форму α-спирали и участвующие в формировании поперечных связей между молекулами эластина. В отличие от коллагена у эластина один генетический тип, мало ОН-ПРО, нет ОН-ЛИЗ, дополнительных пептидов, углеводов, не образуется тройная спираль. Синтезируется эластин в виде мономера, а внеклеточно происходит фибриллогенез с образованием поперечных связей с помощью аминокислоты десмозина — продукта межмолекулярной конденсации 4-х остатков ЛИЗ. Эластин — самый прочный из белков, известных в организме человека. Разрушается под действием фермента эластазы.
Фибриллярные адгезивные белки
Внеклеточный матрикс содержит большое число адгезивных неколлагеновых белков, структурной особенностью которых является наличие доменов, способных специфически связываться с другими макромолекулами и рецепторами на поверхности клетки. Непременным компонентом доменов, обеспечивающих взаимодействие с клетками, является последовательность аминокислот АРГ-ГЛИ-АСП (R-G-D).
Фибронектин — высокомолекулярный гликопротеин. Существуют множественные формы фибронектина. Одна из них — фибронектин плазмы и других биологических жидкостей. Он принимает участие в механизмах свертывания крови и заживления ран. Фибронектины тканей располагаются на поверхности клеток, образуя фибронектиновые филаменты. Фибронектин ускоряет клеточную миграцию, обеспечивая взаимодействие клеток с матриксом.
Фибриллин — структурный компонент микрофибрилл, обеспечивающих образование эластиновых волокон. Он найден в хрусталике, периосте, аорте. При мутации гена, кодирующего синтез фибриллина, развивается синдром Марфана: эктопия хрусталика, арахнодактилия («паучьи» пальцы), поражение суставов.
Ламинин и энтактин — гликопротеины базальной мембраны. Они связываются не только между собой, но и с коллагеном, гепарансульфатом, поверхностью эпителиальных клеток, причем для связывания с различными веществами имеются свои домены.
Каждый тип соединительной ткани имеет свои специфические наборы молекул: кроме соответствующих изоколлагенов, имеются и специфические неколлагеновые белки.
В хрящевой: главный ПГ и минорные ПГ (фибромодулин — регулятор фибриллогенеза; бигликан — значение его пока неизвестно; декорин — способен связываться с коллагеном и играет роль ингибитора фибринолиза; белки с разной молекулярной массой и не очень изученными функциями, из известных функций — связывание с хондроцитами, кристаллами гидроксиапатита, коллагеном II для его фиксации к хондроцитам).
Схематическое строение главного протеогликана хряща:
В костной: индукторы и ингибиторы остеогенеза, инициаторы минерализации — остеокальцин, остеонектин, остеопонтин, костный кислый гликопротеин, костный сиалопротеин, тромбоспондин.