что такое склонность к тромбозам
Тромбоз: причины, симптомы, диагностика, лечение
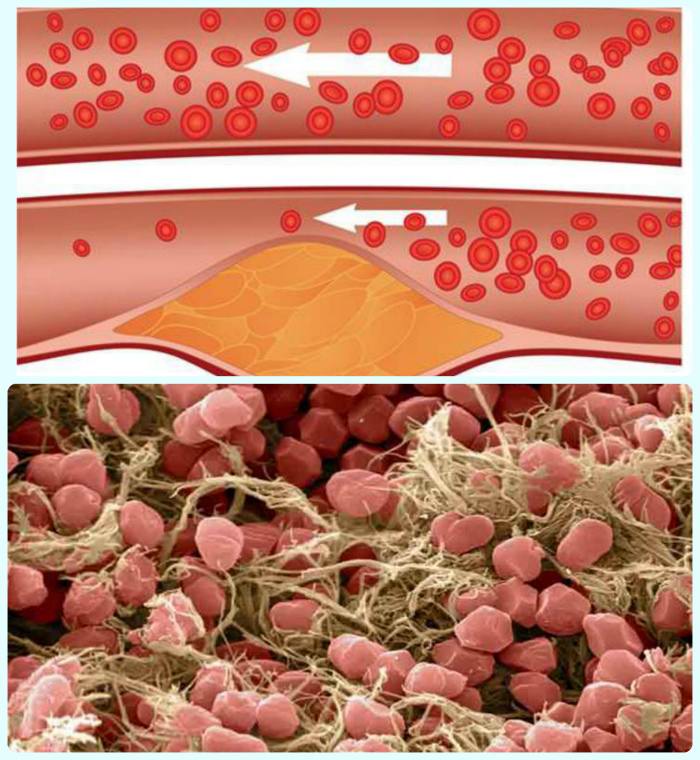
Тромбоз – полная или частичная закупорка просвета сосуда пристеночным или подвижным тромбом. Тромб – это плотный сгусток крови, появляющийся вследствие изменения ее текучести. В норме тромбообразование – защитный механизм. Повреждение сосудистой стенки влечет замедление кровотока, накапливание тромбоцитов вокруг повреждения. Тромб буквально «штопает» стенку сосуда.
Классические причины тромбообразования описываются триадой Вихрова: повреждение сосудистой стенки, замедление кровотока и изменение свойств крови [3]. Некоторые тромбы (их называют эмболами) способны передвигаться до более узких участков сосуда, которые и закупоривает полностью или частично. Ежегодно около 25 млн человек погибают от тромбозов, еще больше сталкиваются с нарушениями трофики, вызванными тромбами [3].
Типы сосудистых тромбозов
Наиболее распространены тромбозы нижних конечностей, однако наибольшую опасность представляют собой тромбоэмболия легочной артерии – ТЭЛА – и синдром диссеминированной внутрисосудистой свертываемости – ДВС-синдром.
Тромбоз артерий развивается при закупорке ее просвета тромбом или эмболом. Клинические признаки определяются местом, где произошла такая закупорка, органом или тканью, плохо снабжающемуся кровью или не снабжающемуся ею вовсе. Если закупорка с нарушением проходимости сосуда происходит медленно, открываются «запасные», коллатеральные, сосуды, что смягчает клинические симптомы артериального тромбоза [3]. Тромбозы артерий чаще возникают у мужчин среднего и пожилого возрастов [7].
Тромбоз вен различается в зависимости от локализации поражения на тромбоз глубоких или поверхностных вен и тромбоэмболию легочной артерии. Среди всех сердечно-сосудистых патологий венозные тромбозы по частоте встречаемости занимают третье место, уступая лишь ИБС и атеросклерозам. Третье место в структуре причин смертности занимает ТЭЛА. Начиная с 40 лет, риск развития венозных тромбозов увеличивается вдвое каждые 10 лет [5].
Описывают два варианта поражения вен нижних конечностей: флеботромбоз (первичный тромбоз, тромб непрочно фиксирован) и тромбофлебит (вторичный тромбоз на фоне воспаления стенки сосуда, тромб фиксирован прочно) [6]. Тромбофлебиты чаще ассоциируются с тромбозом вен поверхностных [2]. Чем более крупная вена пострадала от тромбоза, тем ярче его клинические проявления. Окружающие ткани сдавливаются застоем крови, так как к месту окклюзии кровь пребывает, а по направлению к сердцу не движется. Венозные тромбы склонны отрываться и разноситься с током крови (тромбоэмболы). При их попадании в жизненно важные органы развиваются жизнеугрожающие состояния [3].
Причины тромбоза
Факторы риска образования тромбозов
Клиника тромбоза
Симптомы тромбоза могут быть общими независимо от локализации или специфичными. Общие симптомы включают боль при движении и в покое, ограничение подвижности и снижение функционирования пострадавшего органа или ткани.
Диагностика тромбоза
Первичная диагностика основана на подробном анамнезе и антропометрии (окружность голени или бедра). Используются шкалы Уэллса для диагностики острого тромбоза и диагностики ТЭЛА [8,9].
Инструментальная диагностика включает компрессионное или дуплексное сканирование вен, допплерографию с компрессией вен, импедансную плетизмографию, пульмоноангиографию, рентгеноконтрастную или МРТ-флебографию [6,9], КТ и МРТ-ангиографию [7,9].
Для диагностики артериальных тромбозов применяют физические тесты (тест 6-минутной ходьбы, тредмил тест), определение пульсации поверхностно расположенных артерий (артерии тыла стопы), дуплексное сканирование артерий конечностей, ангиографию (рентгеновский снимок сосуда, заполненного рентгенконтрастным веществом) и измерение транскутанного напряжения кислорода [7].
Анализы при тромбозе
Значительную роль в своевременной диагностике тромбозов играют лабораторные показатели. Так, методические рекомендации по ведению пациентов с новой коронавирусной инфекцией предусматривают стратификацию риска коагулопатии у пациентов с СOVID-19 на основе простых лабораторных тестов: D-димер, протромбиновое время, количество тромбоцитов, уровень фибриногена [1,9].
Клинический анализ крови позволяет выявить воспаление. Он же определяет уровень тромбоцитов, то есть самого субстрата тромбоза.
Дополнительно об уровне воспаления в крови и риске тромбоза свидетельствует повышенный уровень С-реактивного белка.
Биохимический анализ в первую очередь демонстрирует уровень глюкозы крови. По ней можно судить о наличии диабета, одного из серьезнейших факторов риска тромбозов.
Также биохимический анализ способен определить уровень протеина С, что также характеризует выраженность риска тромбоза.
Повышенный уровень гомоцистеина в крови также является доказанным на сегодняшний день риском тромбозов, приводящим к невынашиванию беременности и сердечно-сосудистым событиям (инфарктам и инсультам).
D-димер – лабораторный маркер фибринообразования [8]. Он же говорит о наличии воспаления, как и С-реактивный протеин. Уровень D-димера является контрольным показателем COVID-19 и его осложнений, в том числе связанных с тромбозами.
Можно сдать анализы по комплексной программе «Тромбоз», включающей определение уровней Антитромбин-III, D-димера и генетических факторов кардиологических заболеваний и уровень тромбоцитов. Эта программа позволяет определить факт свершившегося тромбоза где-то в организме, а также определить генетическую предрасположенность к нему. Такую программу, как и прочие анализы, предлагает сеть клиник СИТИЛАБ.
Дополнительное определение уровня гомоцистеина, С-реактивного белка поможет определить биохимический риск тромбоза.
Лечение и профилактика тромбозов
Лечение тромбоза включает антикоагулянтную и антиагрегантную, тромболитическую терапию, установку кава-фильтра нижней полой вены, хирургическое удаление тромба [5]. Необходимо иметь в виду осложнения антикоагулянтной терапии: большое кровотечение, гепарин-индуцируемую тромбоцитопению и варфарин-индуцируемый некроз кожи [5]. Для снижения риска продолжения тромбообразования применяют НПВС [2]. С целью вторичной профилактики назначают небольшие дозы гепарина.
Также назначают немедикаментозные методы лечения – эластичное бинтование, компрессионный трикотаж, локальную гипотермию и ЛФК [2, 4].
Профилактика тромбоза включает ряд мероприятий, применяемых в ситуациях повышенного риска тромбообразования.
Что такое склонность к тромбозам
Тромбофилия – это наследственно обусловленная или приобретенная предрасположенность к формированию тромбов (кровяных сгустков) в просвете кровеносных сосудов. Тромбофилия не является заболеванием как таковым, а представляет собой состояние, которое в сочетании с факторами риска увеличивает вероятность возникновения тромбов в несколько раз.
Проявления тромбофилии связаны с образованием тромбов в венах и/или артериях, которые нарушают работу внутренних органов и представляют серьезную опасность для здоровья и жизни пациента. Однако многие люди с тромбофилией не испытывают в течение жизни никаких негативных последствий этого состояния.
Специфическое лечение тромбофилии отсутствует. Вопрос необходимости использования профилактической терапии, направленной на предотвращение формирования тромбов, решается индивидуально для каждого пациента. При высоком риске тромбоза профилактическое лечение позволяет предотвратить ряд тяжелых осложнений.
Прогноз тромбофилии зависит от ее типа, наличия и тяжести предшествующих случаев тромбоза, сопутствующих заболеваний.
Первичная тромбофилия, наследственная тромбофилия, врождённая тромбофилия, вторичная тромбофилия, приобретенная тромбофилия.
Hypercoagulability, coagulability, hypercoagulable state, hereditary thrombophilia, familial thrombophilia, primary thrombophilia, acquired thrombophilia, secondary thrombophilia.
Тромбофилия – это наследственно обусловленная или приобретенная предрасположенность к формированию тромбов (кровяных сгустков) в просвете кровеносных сосудов. Тромбофилия не является заболеванием как таковым, а представляет собой состояние, которое в сочетании с факторами риска увеличивает вероятность возникновения тромбов в несколько раз.
Проявления тромбофилии связаны с образованием тромбов в венах и/или артериях, которые нарушают работу внутренних органов и представляют серьезную опасность для здоровья и жизни пациента. Однако многие люди с тромбофилией не испытывают в течение жизни никаких негативных последствий этого состояния.
Специфическое лечение тромбофилии отсутствует. Вопрос необходимости использования профилактической терапии, направленной на предотвращение формирования тромбов, решается индивидуально для каждого пациента. При высоком риске тромбоза профилактическое лечение позволяет предотвратить ряд тяжелых осложнений.
Прогноз тромбофилии зависит от ее типа, наличия и тяжести предшествующих случаев тромбоза, сопутствующих заболеваний.
Большинство пациентов не знают о наличии у них тромбофилии до тех пор, пока не возникнет тромбоз или другие нарушения свертывания крови. Чаще всего при появлении тромба появляются следующие симптомы:
Общая информация о заболевании
Тромбофилия представляет собой состояние, при котором сгустки в крови образуются легче, чем в норме. Это происходит за счет изменения соотношения свертывающих и противосвертывающих факторов.
Нормальный процесс свертывания крови необходим для предотвращения кровотечений и заключается в формировании сгустков, которые закупоривают поврежденный сосуд. Процесс формирования сгустка происходит за счет взаимодействия ряда активных веществ – так называемых факторов свертывания. Существуют и противосвертывающие факторы, необходимые для предотвращения избыточного свертывания крови. При тромбофилии баланс этих веществ нарушен – либо повышается количество факторов свертывания, либо снижается количество противосвертывающих веществ. Это может привести к формированию тромбов – сгустков в просвете сосудов (вен или артерий), которые могут закупоривать просвет сосуда, нарушая таким образом кровоснабжение органов и тканей.
Тромбофилии делят на:
1. Врождённые (наследственные, первичные). Это тромбофилии, которые обусловлены наличием аномалий в генах, содержащих информацию о белках, участвующих в свертывании крови. Чаще всего встречается дефицит антитротромбина III, протеинов C и S, аномалия фактора V (мутация Лейден), аномалия протромбина G 202110А:
2. Приобретенные. К ним относятся тромбофилии, которые возникли в результате других заболеваний или приема лекарственных препаратов:
Тромбофилия может встречаться при заболеваниях, сопровождающихся повреждением сосудов, в частности при сахарном диабете, при котором, как известно, уровень инсулина снижен и, как следствие, повышена концентрация глюкозы в крови. Механизм повреждения сосудов при сахарном диабете до конца не выяснен, однако известно, что глюкоза токсически действует на клетки сосудов. Это приводит к выделению факторов свертывания, нарушению тока крови и избыточному тромбообразованию.
Чаще всего тромбофилия проявляется следующим образом.
Кто в группе риска?
Основой диагностики тромбофилий являются лабораторные исследования. Они должны проводиться через несколько недель после перенесенного эпизода тромбоза и вне приема препаратов, влияющих на свертывание крови.
Лечение тромбофилии зависит от степени риска тромбоза. Если он велик и превышает риск развития осложнений от терапии тромбофилии, то врач может назначить:
Специфической профилактики самой тромбофилии нет, однако большое значение имеет предупреждение тромбоза у пациентов с уже диагностированной тромбофилией: контроль за массой тела, рациональное питание, достаточное употребление жидкости (без кофеина, т. к. он сужает сосуды), умеренность в употреблении алкоголя, подвижный образ жизни, отказ от курения, ношение компрессионного белья при варикозе.
Рекомендуемые анализы
Тромбофилия
Термин «гематогенная тромбофилия» объединяет наследственные, генетически предопределённые, и приобретенные (симптоматические, вторичные) нарушения равновесия свёртывания крови, которые рано проявляются появлением и рецидивированием тромбозов, тромбоэмболией, инфарктом и ишемией органов. Это не болезнь, а патологическое состояние, которое обусловлено комбинацией факторов риска, которые приводят к развитию тромбоза.
Причины
Гемостазиологи выделяют 3 фактора, способствующие развитию тромбозов:
Предтромботические состояния называют тромбофилиями. Для них характерна склонность к тромбозам различной локализации даже без повреждения стенки сосуда. Тромбофилии бывают первичными, или врождёнными, и вторичными, развившимися на фоне основного заболевания.
Таблица №1. Генетические аномалии, вызывающие осложнения.
| № п.п. | Генетическая аномалия | Характеристика |
| 1. | Мутационные изменения гена пятого фактора свёртывания | Аутосомно-доминантная мутация гена, который отвечает за продукцию пятого фактора. Она обусловлена заменой остатка аденина в положении 1691 на остаток тимина, и остатка глютамина в позиции 506 на аргинин |
| 2. | Мутация генов протеинов C и S | Наследуется аутосомно-доминантным путём. В результате мутации не заканчивается процесс синтеза или происходит деформация белковые молекулы |
| 3. | Наследственная гипергомоцистеинемия | Происходит мутация генов, которые отвечают за выработку ферментов цистатион-В-синтазы и метилентетрагидрофолатредуктазы |
| 4. | Наследственный дефицит антитромбина III | Наследуется по аутосомно-доминантному пути. Может либо снижаться концентрация этого фактора, либо нарушаться его функция |
| 5. | Мутация гена протромбина G 20210A | Происходит замена гуанина в положении 20210 на остаток аденина, расположенного в нетранслируемом участке гена протромбина. При этом существенно повышается выработка и содержание этого прокоагулянта |
К факторам риска развития тромбофилии относятся:
Риск развития тромбофилии повышен у пациентов, которые получают химиотерапию при злокачественном процессе, лечение прогестероном или эстрогенами, принимают селективные модуляторы эстрагона.
Симптомы
Тромбофилия не проявляется какими-то характерными клиническими симптомами. Основные состояния приобретенной тромбофилии следующие:
У врачей возникает подозрение о наличии у пациента проблем со свёртываемостью крови при появлении следующих признаков претромбоза:
В этих случаях проводят лабораторные исследования системы гемостаза, которые позволяют оперативно выявить и измерить нарастающую тромбогенность крови, требующую коррекции. К лабораторным маркерам тромботической готовности относят активацию тромбоцитов, повышение уровня маркеров активации свёртывания крови и состоявшегося фибринолиза (активированного фактора VII, тканевого фактора, комплекса тромбин-антитромбин). Также в специализированных клиниках проводят тест калиброванной тромбографии. Он позволяет с высокой точностью измерять не только динамику образования, но и инактивацию ключевого фермента свёртывания крови тромбина.
Лечение
У большинства людей, имеющих постоянные или временные факторы риска тромбоза, на протяжении жизни не возникают симптомы нарушения свёртывания крови. Но врачи часто приравнивают наличие факторов тромбогенного риска к тромбофилии. Это приводит к гипердиагностике. Лечения требует не само заболевания, а его осложнения.
Между наличием факторов риска развития тромбофилии и тромбозом существует состояние предтромбоза. Оно заключается в готовности организма проявиться сосудистой катастрофой при сохраняющихся факторах риска. Если у пациента положительные тесты, обнаруживающие факторы тромбогенного риска, гемостазиологи назначают антитромботические препараты. Стратегии профилактики адаптируют к каждому пациенту и каждому ситуационному фактору риска.
Исходники:
Материал размещен в ознакомительных целях, не является медицинским советом и не может служить заменой консультации у врача.
Эксперт
Палишена Елена Игоревна
Врач-терапевт
Специалист по функциональной диагностике,
сертификат №7523,
диплом о медицинском образовании №36726043
Тромбофилия (Генетическая предрасположенность)
“Знать, чтобы предвидеть;
предвидеть, чтобы действовать;
действовать, чтобы предупредить.”
Огюст Конт.
Pro et contra генетического обследования беременных.

В этой статье мы обсудим серьезную проблему наших дней – тромбофилию, ее вклад в акушерские осложнения, гены, предопределяющие развитие тромбофилии у женщины, последствия данного заболевания, способы профилактики и лечения.
Почему мы обсуждаем эту тему? Потому, что нет на свете большего чуда, чем чудо рождения. Мы удивляемся красоте закате и северного сияния, восхищаемся небесным ароматом распустившейся розы. Но все чудеса и загадки нашей планеты, все секреты природы и тайны мира склоняют голову перед рождением: Чудом с большой буквы. Мы должны, мы можем сделать жизнь женщины сказкой со счастливым концом, а не трагедией наподобие жизни NN. Итак, уважаемый доктор, Вашему вниманию предоставляется ключ к лечению бесплодия, выкидышей, аномалий развития и многого другого. Спасти жизнь женщины и будущего ребенка теперь реально осуществимая задача. Новая жизнь в наших руках!
Тромбофилия (ТФ)- это патологическое состояние, характеризующееся повышением свертывания крови и склонностью к тромбозам и тромбоэмболиям. По данным многочисленных исследований это заболевание в 75% является причиной акушерских осложнений.
Классически выделяют два типа ТФ – приобретенные (антифосфолипидный синдром, например) и наследственные. В данной статье речь пойдет о наследственной ТФ и о полиморфных генах (полиморфизмах), ее вызывающих.
Записаться он-лайн на прием к врачам центров МедЛаб в СПб по поводу тромбофилии можно тут: Генетик, Гематолог, Гинеколог, гинеколог-эндокринолог
Генетический полиморфизм не обязательно ведет к состоянию болезни, чаще всего нужны провоцирующие факторы: беременность, послеродовой период, иммобилизация, хирургическое вмешательство, травма, опухоли и тд.
Учитывая особенности физиологической адаптации системы гемостаза к беременности, абсолютное большинство генетических форм тромбофилии клинически проявляется именно в течение гестационного процесса и, как оказалось, не только в форме тромбозов, но и в форме типичных акушерских осложнений. В этот период в организме матери происходит перестройка свертывающей, противосвертывающей и фибринолитической системе, что приводит к увеличению факторов свертывания крови на 200%. Также в III триместре наполовину уменьшается скорость кровотока в венах нижних конечностей из-за частичной механической обструкцией беременной маткой венозного оттока. Тенденция к стазу крови в сочетании с гиперкоагуляцией при физиологической беременности предрасполагает к развитию тромбозов и тромбоэмболий. И при предсуществующей (генетической) ТФ риск тромботических и акушерских осложнений повышается в десятки и сотни раз!
О каком же вреде мы говорим? Как ТФ связана она с акушерскими осложнениями? Все дело в том, что полноценное плацентарное кровообращение зависит от сбалансированного соотношения прокоагулянтных и антикоагулянтных механизмов. Наследственные ТФ приводят к нарушению этого равновесия в пользу прокоагулянтных механизмов. При ТФ снижается глубина инвазии трофобласта, а имплантация неполноценна. Это является причиной бесплодия и ранних предэмбриональных потерь. А нарушение маточно-плацентарного и плодово-плацентарного кровотока вследствие развития тромбозов сосудов является патогенетической причиной таких осложнений, как бесплодие неясного генеза, синдром привычного невынашивания беременности, отслойка нормально расположенной плаценты, преэклампсия, задержка внутриутробного развития плода, синдром потери плода (неразвившаяся беременность, мертворождаемость, неонатальная смертность как осложнение преждевременных родов, тяжелого гестоза, плацентарной недостаточности), HELLP-синдром, неудачные попытки ЭКО.

*Профилактику акушерских осложнений при тромбофилии следует начинать до наступления беременности.
*Родственники больной, имеющие эти же дефекты, должны получать соответствующую профилактику.
*Специфическая профилактика при конкретной мутации (см разделы о полиморфизмах)
Лечение (общие положения)
*Антикоагулянтная терапия независимо от механизма тромбофилии: низкомолекулярный гепарин (не проникает через плаценту, создает низкий риск кровотечений, отсутствие тератогенного и эмбриотоксического эффекта). У женщин с наибольшим риском (генетическая ТФ, тромбозы в анамнезе, рецидивирующие тромбозы) антикоагулянтная терапия показана на протяжении всей беременности. Накануне родов терапию низкомолекулярным гепарином рекомендуется отменять. Профилактика тромбоэмболических осложнений в послеродовом периоде возобновляют спустя 6-8часов и проводят в течение 10-14дней.
*Поливитамины для беременных
*Полиненасыщенные жирные кислоты (омега-3 – полиненасыщенные жирные кислоты) и антиоксиданты (микрогидрин, витамин Е)
*Специфическое лечение при конкретной мутации (см разделы о полиморфизмах)
Критерии эффективности терапии:
*Лабораторные критерии: нормализация уровня маркеров тромбофилии (комплекса тромбин-антитромбин III, Р1+2 фрагмента протромбина, продукты деградации фибрина и фибриногена), числа тромбоцитов, агрегации тромбоцитов
*Клинические критерии: отсутствие тромботических эпизодов, гестоза, плацентарной недостаточности, преждевременной отслойки плаценты
Группы риска:
*беременные с отягощенным акушерским анамнезом (тяжелые формы гестоза, эклампсия, привычное невынашивание беременности и прочие акушерские патологии)
*пациентки с рецидивирующими тромбозами или эпизодом тромбоза в анамнезе или в данную беременность
*пациентки с отягощенным семейным анамнезом (наличие родственников с тромботическими осложнениями в возрасте до 50 лет – тромбозы глубоких вен, тромбоэмболия легочной артерии, инсульт, инфаркт миокарда, внезапная смерть)

Гены системы свертывания крови
ген протромбина (фактор II) G20210A
ген 5 фактора (мутация Лейден) G1691A
ген фибриногена FGB G-455A
ген гликопротеина Ia (интегрин альфа-2) GPIa C807T
ген тромбоцитарного рецептора фибриногена GPIIIa 1a/1b
полиморфизмы, отвечающие за дефицит протеинов С и S, антитромбина III
ген рецептора протеина S PROS1 (большая делеция)
Гены «густокровности»
ген ингибитора активатора плазминогена PAI-1 4G/5G
Гены нарушения тонуса сосудов
ген NO-синтазы NOS3
ген ангиотензинпревращающего фермента ACE (ID)
ген GNB3 С825T
Гены метаболизма
ген метилентетрагидрофолатредуктазы MTHFR C677T
Ген протромбина (фактор II) G20210A
Функция: кодирует белок (протромбин), который является одним из главных факторов системы свертывания
Патология: замена гуанина на аденин в позиции 20210 происходит в нечитаемом участке молекулы ДНК, поэтому изменений самого протромбина при наличии данной мутации не возникает. Мы можем обнаружить повышенные в полтора-два раза количества химически нормального протромбина. Итог – тенденция к повышенному тромбообразованию.
Данные о полиморфизме:
*частота встречаемости в популяции – 1-4%
*частота встречаемости у беременных с венозной тромбоэмболией в анамнезе (ВТЭ) – 10-20%
*аутосомно-доминантное наследование4
Клинические проявления:
*необъяснимое бесплодие, гестозы, преэклампсия, преждевременная отслойка нормально расположенной плаценты, привычное невынашивание беременности, фето-плацентарная недостаточность, внутриутробная гибель плода, задержка развития плода, HELLP-синдром
*венозные и артериальные тромбозы и тромбоэмболии, нестабильная стенокардия и инфаркт миокарда.
Мутация в гене протромбина является одной из наиболее частых причин врожденных тромбофилий, но функциональные тесты на протромбин не могут быть использованы в качестве полноценных скрининговых тестов. Необходимо проводить ПЦР-диагностику с целью выявления возможного дефекта гена протромбина.
Клиническая значимость:
GG-генотип – норма
Наличие патологического A-аллеля (GA, GG- генотип) – повышенный риск ТФ и акушерских осложнений
Дополнительная терапия и профилактика:
*Малые дозы аспирина и подкожные инъекции низкомолекулярного гепарина еще до наступления беременности
При приеме оральных контрацептивов риск тромбозов повышается в сотни раз!
Ген 5 фактора (мутация Лейден) G1691A
Функция: кодирует белок (фактор V), который является важнейшим
компонентом системы свертывания крови.
Патология: Лейденская мутация гена V фактора свертывания крови (замена гуанина на аденин в позиции 1691) приводит к замене аргинина на глутамин в позиции 506 в белковой цепи, являющейся продуктом этого гена. Мутация приводит к устойчивости (резистентности) 5 фактора к одному из главных физиологических антикоагулянтов – активированному протеину C. Результат – высокий риск тромбозов, системной эндотелиопатии, микротромбозов и инфарктов плаценты, нарушения маточно-плацентарного кровотока.
Данные о полиморфизме:
*частота встречаемости в популяции – 2-7%
*частота встречаемости у беременных с ВТЭ – 30-50%
*аутосомно-доминантное наследование
Клинические проявления:
*необъяснимое бесплодие, гестозы, преэклампсия, преждевременная отслойка нормально расположенной плаценты, привычное невынашивание беременности, фето-плацентарная недостаточность, внутриутробная гибель плода, задержка развития плода, HELLP-синдром,
*венозные и артериальные тромбозы и тромбоэмболии.3

Следует помнить, что сочетание лейденской мутации с беременностью, приемом гормональных контрацептивов, повышением уровня гомоцистеина, наличием антифосфолипидных антител в плазме – повышает риск развития ТФ.
Показания к тестированию:
*Повторные ВТЭ в анамнезе
*Первый эпизод ВТЭ в возрасте моложе 50лет
*Первый эпизод ВТЭ с необычной анатомической локализацией
*Первый эпизод ВТЭ развился в связи с беременностью, родами, приемом оральных контрацептивов, гормональной заместительной терапией
*Женщины с самопроизвольным прерыванием беременности во втором и третьем триместре неясной этиологии
Дополнительная терапия и профилактика:
*В случае гетерозиготы (G/A) рецидивы возникают редко, поэтому длительная антикоагулянтная терапия у них проводится лишь при повторном тромбозе в анамнезе
*Малые дозы аспирина и подкожные инъекции низкомолекулярного гепарина еще до наступления беременности, в течение всей беременности и полгода после родов.
Ген метилентетрагидрофолатредуктазы MTHFR C677T
Функция: кодирует фермент метилентетрагидрофолатредуктазу, который является ключевым ферментом фолатного цикла и катализирует
реакцию превращения гомоцистеина в метионин.
Патология: В норме во время беременности уровень гомоцистеина в плазме понижен. Это можно рассматривать, как физиологическую адаптацию организма матери, направленную на поддержание адекватной циркуляции крови в плаценте.
Замена цитозина на тимин в 677 положении приводит к снижению функциональной активности фермента до 35% от среднего значения.
Результат – повышение уровня гомоцистеина в крови, что вызывает эндотелиальную дисфункцию при беременности.
Данные о полиморфизме:
*частота встречаемости гомозиготы в популяции – 1о-12%
*частота встречаемости гетерозиготы в популяции – 40%
*частота встречаемости у беременных с ВТЭ – 10-20%
*аутосомно-рецессивное наследование
Клинические проявления:
*гестоз, преждевременная отслойка нормально расположенной плаценты, задержка внутриутробного развития плода, антенатальная гибель плода
*дефект развития нервной трубки плода (spina bifida), анэнцефалия, умственная отсталость ребенка, «заячья губа», «волчья пасть»
*преждевременное развитие сердечно-сосудистых заболеваний (атеросклероз!), артериальные и венозные тромбозы.
Следует помнить, что данный полиморфизм самостоятельно способен вызывать резистентность 5 фактора к активированному протеину С за счет связывания гомоцистеина с активированным 5 фактором.
Это значит, что он может вызывать все клинические проявления мутации Лейден (см выше).
Дополнительная терапия и профилактика:
*фолиевая кислота (4мг/сутки) в сочетании с витамином В6, В12
*добавление фолиевой кислоты в рацион: содержится в большом количестве в листьях зеленых растений – темно-зеленые овощи с листьями (шпинат, салат-латук, спаржа), морковь, дрожжи, печень, яичный желток, сыр, дыня, абрикосы, тыква, авокадо, бобы, цельная пшеничная и темная ржаная мука.
Ген ингибитора активатора плазминогена PAI-1 4G/5G
Функция: кодирует белок ингибитор активатора плазминогена, который играет важнейшую роль в регуляции фибринолиза, а также является неотъемлемым компонентом в процессе имплантации плодного яйца.
Патология: наличие 4 гуанинов вместо 5 в структуре гена ингибитора активатора плазминогена приводит к повышению его функциональной активности.
Результат – высокий риск тромбозов.
Данные о полиморфизме:
*частота встречаемости в гетерозиготы 4G/5G популяции – 50%
*частота гомозиготы 4G/4G – 26%
*частота встречаемости у беременных с ТФ – 20%
*аутосомно-доминантное наследование

*ранние и поздние выкидыши, развитие ранних и поздних гестозов, преждевременная отслойка нормально расположенной плаценты, фето-плацентарная недостаточность, преэклампсия, эклампсия, HELLP-синдром
*тромбоэмболические осложнения, артериальные и венозные тромбозы, инфаркт миокарда, инсульт, онкологические осложнения
Клиническая значимость:
5G/5G-генотип – норма
Патологический 4G-аллель (4G/4G, 4G/5G – генотип) – высокий риск развития ТФ и акушерских осложнений.
Дополнительная терапия и профилактика:
*низкие дозы ацетилсалициловой кислоты и малые дозы низкомолекулярного гепарина
*низкая чувствительность к терапии аспирином
*витамины антиоксиданты С, Е
*чистая питьевая вода 1,5-2 л/день
Ген фибриногена FGB G455A
Функция: кодирует белок фибриноген (точнее одну из его цепей), вырабатываемый в печени и превращающийся в нерастворимый фибрин – основу тромба при свертывании крови.
Патология: замена гуанина на аденин в 455 положении приводит к повышенной производительности гена, результатом которой становится гиперфибриногенемия и высокий риск развития ТФ, образования тромбов.
Данные о полиморфизме:
Частота встречаемости гетерозиготы (G/A) в популяции – 5-10%
Клинические проявления:
*инсульты, тромбоэмболии, тромбоз глубоких вен нижних конечностей,
*привычное невынашивание беременности, привычные аборты, плацентарная недостаточность, недостаточное поступление питательных веществ и кислорода к плоду 
GG-генотип – норма
Наличие патологического А-аллеля – повышенный риск гиперфибриногенемии, а значит и патологии беременности
Следует помнить, что гиперфибриногенемию вызывает и гипергомоцистеинемия (MTHFR C677T).
Дополнительное лечение и профилактика:
Основной терапией и профилактикой акушерских осложнений в данном случае будет адекватное лечение антикоагулянтами (низкомолекулярный гепарин).
Ген тромбоцитарного рецептора фибриногена GPIIIa 1a/1b (Leu33Pro)
Функция: кодирует бета-3 субъединицу интегрин-комплекса поверхностного рецептора тромбоцитов GPIIb/IIIa, известную также как гликопротеин-3а (GPIIIa). Она обеспечивает взаимодействие тромбоцита с фибриногеном плазмы крови, что приводит к быстрой агрегации (склеиванию) тромбоцитов и, таким образом, к последующему купированию поврежденной поверхности эпителия.
Патология: замена нуклеотида во втором экзоне гена GPIIIa, что приводит к замене лейцина на пролин в 33 положении.
*Происходит изменение структуры белка, что приводит к повышению агрегационной способности тромбоцитов.
*Второй механизм – изменение структуры белка приводит к изменению его иммуногенных свойств, развивается аутоиммунная реакция, что в свою очередь является причиной нарушения свертываемости крови.
Данные о полиморфизме:
*частота встречаемости в популяции – 16-25%

*Артериальные тромботические осложнения
*Усугубляет действие других полиморфизмов, например, мутации Лейден.
Клиническая значимость:
Leu33 Leu33 – генотип – норма
Pro33-аллель – повышенный риск артериального тромбоза
Дополнительная терапия и профилактика
*Антитромбоцитарные препараты нового поколения – антагонисты рецепторов IIb/IIIa – патогенетическая терапия
Ген GNB3 C825T
Функция: является вторичным переносчиком сигнала от рецептора на поверхности клетки в ядро
Патология: точечная мутация в гене G-белка – замена цитозина (С) на тимин (Т) в 825 положении приводит к нарушению функции этого вторичного переносчика. В результате, сигналы перестают поступать в ядро, и нарушается гуморальная регуляция агрегации тромбоцитов.
Клиническая значимость: сам полиморфизм не играет большой роли в патогенезе тромбофилии, однако только при его наличии возможно проявление описанного выше полиморфизма GPIIIa 1a/1b.
Ген NO-синтазы NOS3 (4а/4b)
Функция: кодирует синтазу окиси азота (NOS), которая синтезирует окись азота, принимающую участие в вазодилатации (расслаблении васкулярной мускулатуры), влияет на ангиогенез и свертывание крови.
Патология: наличие четырех повторов нуклеотидной последовательности (4a) вместо пяти (4b) в гене синтазы оксида азота приводит к уменьшению выработки NO, основного вазодилятатора, препятствующего тоническому сокращению сосудов нейронального, эндокринного или локального происхождения.
Данные о полиморфизме:
Частота встречаемости в популяции гомозиготы 4a/4a – 10-20%
Клинические проявления:
Эндотелиальная дисфункция.
Полиморфизм способствует развитию гестоза, преэклампсии, гипоксии плода, задержки внутриутробного развития плода.
Также данный полиморфизм определяет развитие метаболического синдрома, который отрицательно влияет на гормональный фон женщины, что тоже может неблагоприятно отразиться на течении беременности.
Клиническая значимость:
4b/4b – нормальный вариант полиморфизма в гомозиготной форме; 4b/4a – гетерозиготная форма полиморфизма; 4a/4a – мутантный вариант полиморфизма, связанный с увеличением риска заболеваний, в гомозиготной форме
Дополнительное лечение и профилактика:
Патогенетического лечения на данный момент нет. Однако следует помнить, что такой полиморфизм усугубляет клиническую картину других полиморфизмов, повышающих риск тромботических осложнений.
Возможно назначение вазодилятаторов для улучшения кровоснабжения плода, однако исследований по этому вопросу еще не проводилось.
Для профилактики метаболического синдрома и при наличии у беременной избыточного веса, инсулинорезистентности, дислипидемии необходимо назначить диету – нормокалорийную сбалансированную и нормокалорийную несбалансированную по соли. Полиморфизм предопределяет развитие у человека артериальной гипертензии, поэтому полезно назначение физической нагрузки – кардиотренировки – не только во время, но обязательно после беременности.
Ген гликопротеина Ia (интегрин альфа-2) GPIa C807T
Функция: гликопротеин Ia является субъединицей тромбоцитарного рецептора к коллагену, фактору Виллебранда, фибронектину и ламинину. Взаимодействие рецепторов тромбоцита с ними приводит к прикреплению тромбоцитов к стенке поврежденного сосуда и их активации. Таким образом, гликопротеин Ia играет важную роль в первичном и вторичном гемостазе.
Патология: замена цитозина на тимин в 807 положении приводит к повышению его функциональной активности. Происходит увеличение скорости адгезии тромбоцитов к коллагену 1 типа.
Результат- повышение риска тромбоза, инсульта, инфаркта миокарда
Данные о полиморфизме:
*частота встречаемости в популяции – 30-54%
Клинические проявления:
*кардиоваскулярные заболевания, тромбозы, тромбоэмболии, инфаркт миокарда,
*мягкая тромботическая тенденция (усиление действия других полиморфизмов, предрасполагающих организм к тромбофилии)
Клиническая значимость:
СС-генотип – норма
Т-аллель – повышенный риск тромбообразования и патологии беременности
Дополнительное лечение и профилактика:
Патогенетического лечения на сегодняшний день не разработано.
Ген ангиотензинпревращающего фермента ACE (ID)
Функция: превращение неактивной формы ангиотензиногена в ангиотензин
Патология: делеция (deletion D) и вставка (insertion I) нуклеотидной последовательности в гене ангиотензинпревращающего фермента. При наличии у человека D-аллеля повышается риск развития эндотелиальной дисфункции.
Эндотелиальная дисфункция определяет тромботическую тенденцию организма.

Венозные тромбозы и тромбоэмболические осложнения, преждевременные роды, синдром потери плода
Клиническая значимость:
II-генотип – норма
D- аллель – повышает риск развития эндотелиальной дисфункции, являющейся основой всех вышеописанных акушерских осложнений.
Дополнительное лечение и профилактика:
Патогенетической терапии не разработано. Однако следует помнить, что D-аллель этого гена усиливает патологические проявления других предрасполагающих к тромбофилии полиморфизмов.
Также необходимо знать, что данный полиморфизм (D-аллель) является генетическим компонентом метаболического синдрома, наличие которого нарушает гормональный фон женщины. Это, безусловно, может неблагоприятно воздействовать на течение беременности. Поэтому для предотвращения развития метаболического синдрома или при наличии у женщины избыточной массы тела, инсулинорезистентности, дислипидемии следует назначить такой пациентке нормокалорическую диету несбалансированную по липидам и адекватную физическую нагрузку (плаванье, йога и тд).
Полиморфизмы, отвечающие за дефицит протеина С
Функция: протеин С является основным ингибитором тромбоза. Вместе с другими компонентами образуют комплекс, препятствующий избыточному тромбообразованию.
Патология: Потеря взаимодействия между этим антитромботическим комплексом и факторами каскада свертывания ведет к нерегулируемой прогрессии каскада свертывания и избыточному тромбообразованию.
Данные по дефициту протеина С:
*частота встречаемости в популяции – 0,2-0,4%
*частота встречаемости у беременных с ВТЭ – 1-5%
Клинические проявления:
*тромбозы, тромбоэмболии (легочной артерии в частности), поверхностные рецидивирующие тромбофлебиты
*микротромбозы плаценты и соответствующие нарушения фетоплацентарного кровотока
*неонатальная, коагулопатия; синдром неонатальной фульминантной пурпуры (проявляется экхимозами вокруг головы, туловища, конечностей, часто сопровождается церебральными тромбозами и инфарктами; многочисленные кожные изъязвления и некрозы)5
Клиническая значимость:
Полиморфизмов, предопределяющих дефицит протеина С, известно множество, однако неизвестен полиморфизм, определяющий патологию с высокой вероятностью. Поэтому ведущим методом выявления патологии является биохимический анализ крови.
Концентрация 0,59-1,61 мкмоль/л – норма
Концентрация 30-65% от нормы (менее 0,55 мкмоль/л)- гетерозиготный дефицит протеина С
Дополнительная терапия и профилактика:
*инфузия концентрата протеина С или активированного протеина S
*при дефиците протеина С рецидивы возникают редко, поэтому длительная антикоагулянтная терапия у них проводится лишь при повторном тромбозе в анамнезе
*возможно развитие некрозов кожи и подкожной жировой клетчатки при приеме непрямых антикоагулянтов
*одновременно с варфарином необходимо применять низкомолекулярный гепарин
Полиморфизмы, отвечающие за дефицит протеина S
Функция: протеин S является основным ингибитором тромбоза. Вместе с другими компонентами образуют комплекс, препятствующий избыточному тромбообразованию.
Патология: Потеря взаимодействия между этим антитромботическим комплексом и факторами каскада свертывания ведет к нерегулируемой прогрессии каскада свертывания и избыточному тромбообразованию
Выделяют три типа дефицита протеина S: снижение антигенного уровня протеина S, как общего, так и свободного, снижение активности протеина S (1 тип), снижение активности протеина S при его нормальном антигеном уровне (2тип), нормальный общий антигенный уровень протеина S при уменьшении активности (3 тип)
Данные по дефициту протеина S:
*частота встречаемости у беременных с ВТЭ – 2-10%
*аутосомно-доминантный тип обследования
Клинические проявления:
*поверхностные тромбофлебиты, тромбозы глубоких вен, тромбоэмболии легочных артерий, артериальные тромбозы
*спонтанные аборты, внутриутробная гибель плода
Клиническая значимость:
На сегодняшний день известно множество мутаций, предрасполагающих организм к дефициту протеина S, однако выделить из них тот полиморфизм, который является ведущим, пока не представляется возможным.
Совсем недавно открыт полиморфизм, в 95% случаях вызывающий дефицит протеина S первого типа. Это мутация в гене рецептора протеина S PROS1 (большая делеция). Однако роль данной мутации в развитии акушерской патологии пока не достаточно ясна.
Для выявления данной патологии следует проводить биохимический анализ крови.
Дополнительная терапия и профилактика:
*при дефиците протеина S рецидивы возникают редко, поэтому длительная антикоагулянтная терапия у них проводится лишь при повторном тромбозе в анамнезе
*прием варфарина может вызывать некрозы кожи и подкожной жировой клетчатки
Полиморфизмы, отвечающие за дефицит антитромбина III
Функция: антитромбин III является основным ингибитором тромбоза. Вместе с другими компонентами образует комплекс, препятствующий избыточному тромбообразованию.
Патология: Потеря взаимодействия между этим антитромботическим комплексом и факторами каскада свертывания ведет к нерегулируемой прогрессии каскада свертывания и избыточному тромбообразованию.
Наследственный дефицит антитромбина III может проявляться либо снижением синтеза этого белка (тип I), либо нарушением его функциональной активности (тип II)
Данные по дефициту антитромбина III:
*частота встречаемости в популяции – 0,02%
*частота встречаемости у беременных с ВТЭ – 1-5%
*аутосомно-доминантное наследование
Клинические проявления:
*дефицит антитромбина у новорожденного – высокий риск развития респираторного дистресс-синдрома, внутричерепных кровоизлияний
*тромбозы глубоких вен нижних конечностей, почечных вен и вен сетчатки
*микротромбозы плаценты; нарушение фетоплацентарного кровотока
Клиническая значимость: На данный момент выявлено большое количество мутаций, определяющих дефицит антитромбина III. Однако для их проявления необходимо их сочетание. Сегодня неизвестно такой мутации, которая бы определяла дефицит антитромбина III с очень высокой вероятностью. Поэтому диагностика данной мутации проводиться по биохимическим показателям (биохимический анализ крови).
Дополнительная терапия и профилактика:
1) инфузии концентрата антитромбина III;
2) следует помнить, что у больных с такой мутацией тромбозы рецидивируют очень часто, и поэтому, после первого проявления ТФ они должны получать антикоагулянтную терапию пожизненно.
Лабораторные признаки:
*агрегация тромбоцитов в норме
*время кровотечения нормальное
*глобальные тесты коагуляции не изменены
*низкий иммунологический уровень антитромбина III
*низкий уровень биологической активности
*отсутствие адекватного удлинения АЧТВ при гепаринотерапии
*тесты на фибринолиз в норме
Особенно опасные комбинации полиморфизмов: 
*А-аллель гена 5 фактора (мутация Лейден G1691A) + А-аллель гена протромбина (G20210A) + Т-аллель гена MTHFR (C677T)
*А-аллель гена 5 фактора (мутация Лейден G1691A) + дефицит протеина С или протеина S
*А-аллель гена 5 фактора (мутация Лейден G1691A) + делеция в гене PROS1
*Т-аллель MTHFR (C677T) + A-аллель FGB (G455A)
*4G/4G в гене PAI-1 + Т-аллель MTHFR (C677T)
*Pro33-аллель GPIIIa + Т-аллель гена GNB3 (C825T)
Вывод:
генетическое обследование позволит Вам
1. выявить предрасположенность женщины к развитию тромбофилии во время беременности
2. назначить патогенетическую терапию, имеющую наибольшую эффективность в каждом конкретном случае
3. избежать большинства акушерских осложнений, включая бесплодие и внутриутробную гибель плода
4. предотвратить тромботические осложнения у женщины в послеродовом периоде и в последующие годы жизни
5. предотвратить тромботические осложнения у новорожденного
6. предотвратить тератогенное действие тромбофилии (избежать spina bifida e.s.)
7. сделать жизнь женщины счастливой и полноценной.
Генетика способна помочь Вам, дорогой доктор, в исполнении Вашей святой обязанности. Обращайтесь, ждем Вас.
1. Существует более сложная клиническая классификация, основанная на клинических проявлениях ТФ:
2. Полиморфизм – вариант гена, сформированный из точечной приспособительной мутации и закрепленный в нескольких поколениях и встречающийся в популяции более 1-2 процентов.
3. Недавнее исследование показало, что у носителей лейденской мутации частота успеха подсадок зародышей при ЭКО примерно в 2 раза выше, чем среди пациенток, не являющихся носителями данной мутации. Эти любопытные данные указывают на то, что, несмотря на повышенную вероятность развития осложнений, фертильность пациенток с лейденской мутацией (вероятность наступления беременности в каждом цикле) может быть выше.
4. наследование: может быть доминантное и рецессивное (в данной статье не идет речи о наследовании, сцепленном с полом, то есть с половой хромосомой). Доминантное проявится у ребенка при наличии соответствующего гена хоты у одного из родителей, а рецессивное требует одинаковых по данному признаку генов у обоих родителей.
5. синдром описан у людей, дважды гомозиготных по типу 1 (количественный и функциональный дефицит протеина С) и типу 2 (качественный дефицит протеина С); синдром рефрактерен к терапии гепарином или антиагрегантами. Если у больного отсутствуют клинические и лабораторные данные за необратимое повреждение головного мозга или органа зрения, то оптимальной терапией будет использование концентрата активированного протеина С, протеина С или свежезамороженной плазмы в сочетании с гепарином.