что такое сероконверсия при коронавирусе
Бессимптомная сероконверсия иммуноглобулинов при SARS-CoV-2-инфекции и как она может уберечь медперсонал от COVID-19.
Ранее сообщалось, что отделения гемодиализа госпиталей подвержены высокому риску распространения инфекционных заболеваний. Причинами называют невозможность соблюдать социальное дистанцирование в открытых отсеках, большое числа сменяющих друг друга пациентов, а также значительное число процедур как при подготовке к гемодиализу, так и во время его проведения.
Целью исследования, проведённого на базе отдельно стоящего амбулаторного педиатрического отделения для гемодиализа с пятью койками и тремя изолированными помещениями в Riley Hospital for Children, Indianapolis, USA и опубликованного в JAMA, было измерить уровни серийных антител против SARS-CoV-2 у пациентов, медсестер, врачей и обслуживающего персонала, присутствовавших при проведении гемодиализа у пациента с симптомами вирусной инфекции.
Начать проведение данного исследования было решено после того как стало известно, что 7 дней назад (день 0) у одного из пациентов наблюдались лихорадка и общие симптомы вирусного заболевания. Результат ПЦР теста на SARS-CoV-2 в мазке из носоглотки оказался положительным, и оставался положительным при повторных тестах на 7, 14 и 19 день. Сеансы гемодиализа ему проводились в изолированной комнате, начиная со дня 0. При этом весь персонал отделения и пациенты, которым производился гемодиализ, всегда были в масках.
Измерения уровня сывороточного IgM и IgG в сыворотке из образцов цельной крови были произведены у 13 пациентов, проходивших гемодиализ в отделении, у 11 медсестер и 10 врачей отделения, а также у 4 человек из обслуживающего персонала на 7, 14 и 21 дни от начала исследования. Сероконверсией считались положительные анализы на IgM или IgG.
Между 0-м и 7-м днем у 2 человек из медицинского персонала отмечались симптомы вирусного заболевания верхних дыхательных путей и лихорадка при отрицательных результатах ПЦР теста. В дальнейшем один из них сероконвертировал на 21-й день, несмотря на 3 отрицательных результата ПЦР. У остальных участников исследования не проводилось назофарингеальное тестирование на SARS-CoV-2 и не было симптомов COVID-19 до 7-го дня.
К 21 дню у 11 из 25 сотрудников отделения (44%) и у 3 из 13 пациентов (23%) были обнаружены положительные антитела к SARS-CoV-2. При том, что ни у одного из участников исследования между 7 и 21 днями не наблюдалось симптомов заболевания. У одного человека из медицинского персонала, который непосредственно опекал ПЦР-положительного пациента и у двух из 11 медицинских работников, которые ухаживали за 2 двумя пациентами с субклинической сероконверсией, в дальнейшем были обнаружены антитела против SARS-CoV-2. Все они оставались бессимптомными, несмотря на то, что у одного из них всё же был положительным результат теста на ПЦР в мазке из носоглотки.
Данное исследование продемонстрировало высокую распространенность субклинической сероконверсии у лиц, находящихся в контакте с возможными носителями SARS-CoV-2. Это дает надежду, что большее число работников здравоохранения может быть антитело положительными, чем можно было бы ожидать. Информация о серопревалентности медсестер и врачей позволит стратегически правильно укомплектовать персонал по уходу за SARS-CoV-2-позитивными больными и пациентами с подозрением на положительную реакцию, и тем самым уменьшить риск заражения, которому подвергаются медицинские работники в период пандемии COVID-19.
Поскольку это исследование имеет небольшой размер выборки и короткое последующее наблюдение, необходимы более масштабные исследования данной проблемы.
Иммунный ответ на коронавирус SARS-CoV‑2 у больных COVID‑19
Академик Российской академии наук, д.м. н., президент
ФБГУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
В статье представлен анализ результатов исследований иммунного ответа и памяти к SARS-CoV‑2, включая все ветви адаптивного иммунитета, иммуноглобулины, В-клетки памяти, CD8+- и CD4+-T-клетки у больных в динамике в течение 6–8 месяцев после начала заболевания.
Гуморальное звено
Факт первичного иммунного ответа слизистых на COVID‑19 необычен и требует объяснения. Обсуждаются две гипотезы.
Первая: вирусы контаминируют слизистые дыхательных путей и ЖКТ за 7–14 дней до появления системного ответа и клинических проявлений инфекции, поражая клетки микробиоты — используют их для репродукции вируса.
Вторая: кросс-реактивная продукция антител, предпосылкой которой являются Spike-реактивные CD4+-Т-клетки, обнаруженные у большинства пациентов с COVID‑19 и более чем у 34 % неинфицированных людей. Это подтверждает существование общих эпитопов эндемичных коронавирусов, вызывающих банальные ОРВИ и COVID‑19.
Важно, что изотипы иммуноглобулинов (либо IgG, либо IgA) конкурировали за нейтрализующую активность по отношению к SARS-CoV‑2 в зависимости от локализации. Сывороточные антитела IgG сильно коррелировали с величиной IgG-ответа и тяжестью заболевания. У пациентов, например, с IgA-назальным ответом определялась высокая активность нейтрализации вирусов. Инфекция у таких больных протекала бессимптомно.
Это, с одной стороны, предполагает возможность нейтрализации вируса с помощью IgA слизистых без системного ответа, что имеет отношение к исходам заболевания. А с другой стороны, из-за множества корреляций, наблюдаемых между типами антител и их активностью в разных анатомических участках, клиническая интерпретация гуморального ответа существенно затруднена.
Кроме того, эти данные имеют важное значение для нашего понимания защиты вакцинации, индуцирующей системный ответ на вакцинные гены или белки коронавируса по классическому пути и обеспечивающей иммунный ответ слизистых оболочек на 3–6‑й неделе после вакцинации. В идеале вакцина должна не только защитить реципиента от неизбежной болезни, но и предотвратить бессимптомное носительство, что закрыло бы проблему бессимптомных носителей в популяции.
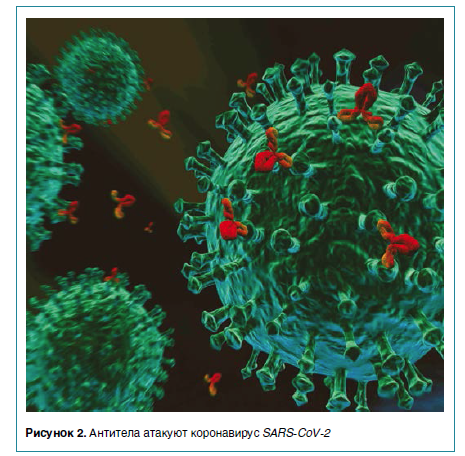
Титры Spike IgА и RBD IgА сохранялись на стабильном уровне на протяжении всего периода наблюдения t1/2— 210 дней, но у отдельных пациентов уровень специфических IgА-антител достоверно снижался через 90 дней.
Нельзя дать однозначный ответ в отношении серонегативных случаев COVID‑19. По-видимому, кроме протективного эффекта иммунитета слизистых, ответ напрямую связан с уровнем вирусной нагрузки SARS-CoV‑2. С одной стороны, высокие вирусные нагрузки связаны с более ранним ответом антител, в то время как у пациентов с низкой вирусной нагрузкой не может быть сероконверсии. С другой стороны, кинетика иммунного ответа может быть показателем скорости элиминации вируса у больного.
Идентификация специфичных В-клеток памяти к Spike, RBD и NCP с использованием флюоресцентно окрашенных зондов на IgD– и (или) CD27+ c последующей дифференцировкой по изотипам поверхностных IgM, IgG или IgA показала следующее. Количество специфических В-клеток увеличивалось в течение 120 дней после начала заболевания с последующим выходом на плато, в то время как Spike-специфические В-клетки памяти у людей, не заболевших COVID‑19, практически не встречались. RBD-специфические В-клетки появлялись на 16‑й день, и их количество увеличивалось в течение последующих 4–5 месяцев. Интересно, что только 10–30 % Spike-специфических В-клеток памяти было специфично для домена RBD через 6 месяцев после выздоровления больных.
NCP-специфичные В-клетки памяти также стабильно увеличивались в те же сроки и определялись спустя 5–6 месяцев после заболевания. Представленность изотипов иммуноглобулинов Spike-специфических В-клеток имела следующую динамику. В ранней фазе (20–60 дней) после заболевания IgM+ и IgG+ на В-клетках были представлены одинаково. В период после 60 дней до 240‑х суток преобладали IgG+ Spike-специфические В-клетки. Частота IgА+ Spike-специфических клеток составляла примерно 5 %, и они равномерно распределялись в течение всего периода наблюдения в 8 месяцев. Корреляция между сывороточным IgA и IgA слизистых оболочек не проводилась.
Сходная картина динамики наблюдалась и в случае IgG+, IgM+ и IgА+ к эпитопам RBD и NCP коронавируса. В то же время долгосрочное присутствие циркулирующих В-клеток памяти, направленных как против основных SARS-CoV‑2‑нейтрализующих таргетов (Spike и RBD), так и против не нейтрализующего таргета (NCP), свидетельствует о клеточной памяти, сохраняющейся после естественного воздействия вируса. Это может быть использовано для планирования ревакцинации. Тот факт, что почти все RBD- специфические IgG+-В-клетки памяти экспрессировали CD27, свидетельствует о долгосрочной иммунной памяти.
Анализ полученных данных говорит о том, что снижение нейтрализующих и других антител к SARS-CoV‑2 после клинического выздоровления вовсе мунитета. Просто с развитием и сохра- нением памяти В-клеток, способных активизироваться при встрече с новыми штаммами коронавируса, уровень антител в сыворотке снижается, в то время как IgА-ответ слизистых сохраняется на постоянном уровне в течении всего периода наблюдения.
Клеточный ответ
Процент больных с обнаруживаемыми циркулирующими CD8+-Т-клетками памяти через месяц после возникновения симптомов составил 70 %. К 6–9 месяцам клетки обнаруживались у 50 % выздоровевших пациентов. Фенотипические маркеры показали, что большинство SARS-CoV‑2‑специфичных CD8+-Т-клеток представлены терминально дифференцированными клетками памяти.
Циркулирующие SARS-CoV‑2‑специфичные CD4+-Т-клетки памяти через месяц после начала заболевания обнаруживались у 93 % пациентов. Через 6–9 месяцев уровень этих клеток был стабильным, а сами они выявлялись у более чем у 90 % пациентов, перенесших COVID‑19. Причем это касалось как Spike-специфичных, так и мембраноспецифичных CD4+-Т-клеток памяти.
Интересно, что при сравнении параметров иммунного ответа у больных с тяжелым и легким течением инфекции гуморальные показатели были более высокими у тяжелых больных, в то время как CD8+-Т-клетки были стабильными, а CD4+ — более низкими в тяжелых случаях заболевания. Объяснений этому феномену нет, важно, что слабый ответ Т-клеток наблюдается в острой фазе заболевания. Кроме того, важна и методология исследования клеточного им-мунитета.
Нарушения клеточного ответа проиллюстрированы дефицитом интерферонов I и II типов у пациентов с тяжелыми и среднетяжелыми формами COVID‑19 по сравнению с легкими и бессимптомными случаями заболевания. Это может быть связано с подавлением воспаления интерлейкином‑12 (IL‑12) и развитием вторичного дефекта клеточного иммунитета.
Иммунное взаимодействие
Большой интерес представляет изучение взаимодействия гуморального и клеточного ответа на SARS-Cov‑2. В исследованиях RBD-IgG, Spike IgА, RBD-В-клеток памяти, CD8+- и CD4+-Т-клеток в динамике у одних и тех же пациентов установлено, что у большинства из них (64 %) положительные показатели отмечались через 1–2 месяц после начала заболевания. Через 5–8 месяцев число реконвалесцентов, позитивных на пять тестов, снизилось до 43 %. В то же время как минимум три из пяти тестов были положительными спустя 6–9 месяцев. Важно отметить, что IgG на Spike дает на порядок больше положительных ответов, чем на RBD-антиген. Попытки связать гуморально- клеточные взаимодействия не привели к успеху из-за неоднородности участников исследования и методик оценки иммунного ответа.
Неопределенный результат
В метаанализе 22 исследований (4969 пациентов) установлены неблагоприятные признаки тяжелых форм болезни и летальных исходов, такие как лимфопения и нейтрофилез. Поскольку CD4+-Т-клетки необходимы для сбалансированного и эффективного иммунного ответа, неудивительно, что низкий уровень лимфоцитов может отражать гипервоспалительные процессы и способствовать более тяжелому течению заболевания и повышенной смертности.
Нейтрофилы как неотъемлемая часть врожденной защиты контролируют баланс микробиоты и элиминацию продуктов клеточной деструкции за счет производства активных форм кислорода и высвобождения нейтрофильных внеклеточных ловушек в венозном кровотоке. Лимфопения (менее 500 клеток в 1 мкл) указывает на повышение риска тяжелой формы заболевания и смертельных исходов при COVID‑19 в 3 раза. Стойкий нейтрофилез со сдвигом влево свидетельствует об истощении костномозгового резерва, а при сдвиге вправо отражает нарушения выхода клеток в ткани. Этот легко контролируемый анализом крови параметр указывает на более чем семикратное увеличение для пациента риска заболеть тяжело и погибнуть от COVID‑19.
Попытки выявить закономерности иммунного ответа на SARS-CoV‑2 оказались пока безуспешными.
Во-первых, можно сделать вывод, что переболевшие коронавирусной инфекцией сохраняют иммунную память в последующие 6–9 месяцев. Дальнейшие динамические исследования покажут, в какие сроки наступает снижение иммунного ответа, требующее профилактической вакцинации и (или) ревакцинации.
Во-вторых, и это очень интересно, каждый изученный компонент иммунного ответа и иммунной памяти демонстрирует различную кинетику. Это связано с индивидуальным ответом на инфекцию, наличием преморбида и частого превращения моноинфекции в смешанные инфекции SARS-CoV‑2 с активизировавшейся микробиотой больного.
В-третьих, неоднородность ответа может быть центральным признаком, характеризующим иммунную память к SARSCoV‑2. Биологические специфические IgG имеют 21 день периода полураспада, уровень антител с течением времени отражает продукцию короткоживущих, а потом и долгоживущих плазматических клеток. С точки зрения исчезновения возбудителя в течение нескольких дней после появления клиники, процесс наработки антител должен быть снижен к 6 месяцам, но, если SARS-CoV‑2 Spike и RBD IgG сохраняются дольше 8 месяцев, это означает, что вирус персистирует в организме хозяина или его микробиоте. Нельзя исключать и связь с пролонгированным иммунным ответом естественной реиммунизации циркулирующими эпидемическими альфа-коронавирусами, поддерживающими иммунный ответ.
В-четвертых, выявление и анализ SARSCoV‑2‑специфических В-клеток памяти потенциально могут применяться в качестве маркера гуморального ответа при вакцинации. Сейчас исследования поствакцинального иммунного ответа проводятся с использованием иммунофлуоресцентного анализа с оценкой IgM- и IgG-антител в качестве маркеров эффективности вакцины (рис. 3). Методы ИФА-диагностики, к сожалению, не стандартизованы едиными белками S, RBD, NCP, качество которых зависит от очистки антигена. Поскольку количество В-клеток памяти стабильно с течением времени, они могут представлять собой более надежный маркер продолжительности гуморальных иммунных реакций, чем иммуноглобулины сыворотки крови.
Таким образом, из результатов исследований иммунного ответа у больных COVID‑19 невозможно сделать какие-либо выводы о защитном иммунитете при новой коронавирусной инфекции. Ведь изучение антител и клеток памяти при этом заболевании пока еще не завершено. А значит, обсуждаемые механизмы защитного иммунитета против SARS-CoV‑2 у людей окончательно не определены.
Источник: Газета «Педиатрия сегодня» №6, 2021
Обнаружившая коронавирус «Омикрон» врач описала «необычные» симптомы
Названы группы риска для новой мутации COVID-19
«Необычные» симптомы мутантного штамма COVID-19 «Омикрон» описала доктор из ЮАР, которая первой в мире подняла тревогу по поводу варианта «Омикрон». По словам доктора Кутзее, к новым проявлениям заболевания относятся учащенный пульс и сильная усталость, при этом ни у одного из ее пациентов не было типичной потери вкуса или запаха.
Южноафриканская врач, которая первой забила тревогу по поводу нового варианта COVID-19 «Омикрон», обнаружила, что у пациентов проявляются «необычные» симптомы.
Как пишет Daily Mail, доктор Анжелика Кутзее, которая имеет частную практику в административной столице ЮАР Претории, рассказала, что она впервые заметила ранее в ноябре, что пациенты с COVID-19 проявляют ряд странных симптомов.
Врач, практикующая более тридцати лет и возглавляющая Южноафриканскую медицинскую ассоциацию, говорит, что ни один из пациентов с вариантом «Омикрон» не страдал от потери вкуса обоняния, обычно связываемой с коронавирусом, но вместо этого у него были такие необычные симптомы, как сильная усталость и высокая частота пульса.
«Их симптомы были настолько разными и такими легкими по сравнению с теми, что я лечила раньше», – сообщила доктор Кутзее изданию The Telegraph. Она сообщила о своих наблюдениях консультативному совету Южной Африки по вакцинам 18 ноября, когда лечила семью из четырех человек, которые все страдали от сильной усталости после положительного результата теста на COVID-19.
Судя по выводам врача из ЮАР, вероятность осложнений при заражении вариантом «Омикрон» может угрожать пожилым людям, страдающим диабетом или сердечно-сосудистыми заболеваниями.
Новый вариант коронавируса «Омикрон», впервые обнаруженный в Южной Африке в начале ноября, с тех пор был обнаружен в Великобритании, Германии, Италии, Бельгии, Ботсване, Израиле, Гонконге, Австралии и других странах.
Открытие «Омикрона», которое Всемирная организация здравоохранения (ВОЗ) назвала «вариантом беспокойства», вызвало опасения во всем мире, что эта мутация может сопротивляться вакцинации и продлить почти двухлетнюю пандемию коронавируса. «Омикрон» потенциально более заразен, чем предыдущие варианты, хотя эксперты еще не знают, вызовет ли он более или менее серьезный COVID-19 по сравнению с другими штаммами.
Доктор Кутзее заверила СМИ, что новые симптомы, которые она наблюдала, были «легкими» и что все пациенты, которых она лечила, выздоровели. «У нас был один очень интересный случай: ребенок лет шести, с температурой и очень частым пульсом, и я подумала, следует ли мне принимать ее, – рассказала доктор Кутзее. – Когда я наблюдала через два дня, ей стало намного лучше».
Но врач из ЮАР при этом сказала, что она обеспокоена тем, что вариант может представлять большую опасность для пожилых людей.
Обнаружение нового варианта коронавируса побудило несколько стран усилить связанные с COVID ограничения и ввести строгий пограничный контроль в попытке сдержать распространение.
Главный медицинский советник британского правительства Крис Уитти заявил, что пока неясно, насколько эффективны существующие вакцины в качестве защиты от варианта «Омикрон», но сказал, что вакцинированные или прошедшие ревакцинацию люди с меньшей вероятностью серьезно заболеют. По его словам, новый вариант коронавируса «неизбежно» распространится по всему миру в течение следующих нескольких дней, но добавил, что большинство случаев в Великобритании по-прежнему относятся к варианту «Дельта». Он предупредил, что в настоящее время высокие показатели передачи инфекции наблюдаются среди молодежи, но отметил, что показатели среди людей старше 60 лет и уязвимых групп улучшаются, а это означает, что количество госпитализаций и смертей продолжает снижаться.
Интерпретация диагностических тестов на SARS-CoV-2
Пандемия коронавирусной инфекции 2019 года (COVID-19) продолжает оказывать свое влияние на весь мир. Знания о диагностических тестах на SARS-CoV-2 по-прежнему расширяются, и крайне важным является понимание смысла этих тестов и правильная интерпретация их данных. Этот материал объясняет, как интерпретировать два типа диагностических тестов, обычно используемых для диагностики инфекции, вызванной SARS-CoV-2 — ПЦР с обратной транскрипцией и ИФА для определения IgG и IgM — и как их результаты могут изменяться с течением времени.
.
Определение вирусной РНК методом обратной транскрипции
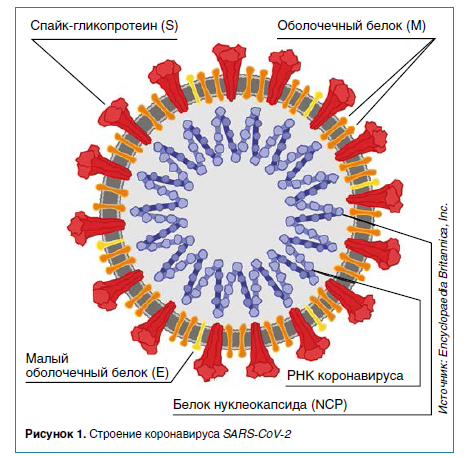
На сегодняшний день наиболее часто используемый и достоверный тест для диагностики COVID-19 — это ПЦР с обратной транскрипцией. В качестве материала для исследования чаще всего используют мазок из носоглотки или реже другие образцы из верхних дыхательных путей, например, мазок из ротоглотки или слюну. Производители используют разные целевые гены в структуре РНК, но большинство тестов определяет наличие таких генов, как env, spike (S), ORF1, ген нуклеокапсида (N) и ген РНК-зависимой РНК полимеразы (RdRp). По данным сравнительного исследования, тесты сопоставимо чувствительны к различным индивидуальным генам; исключение составляет зонд RdRp-SARSr, который обладает меньшей чувствительностью (вероятно, из-за несоответствия нуклеотидов в обратном праймере).
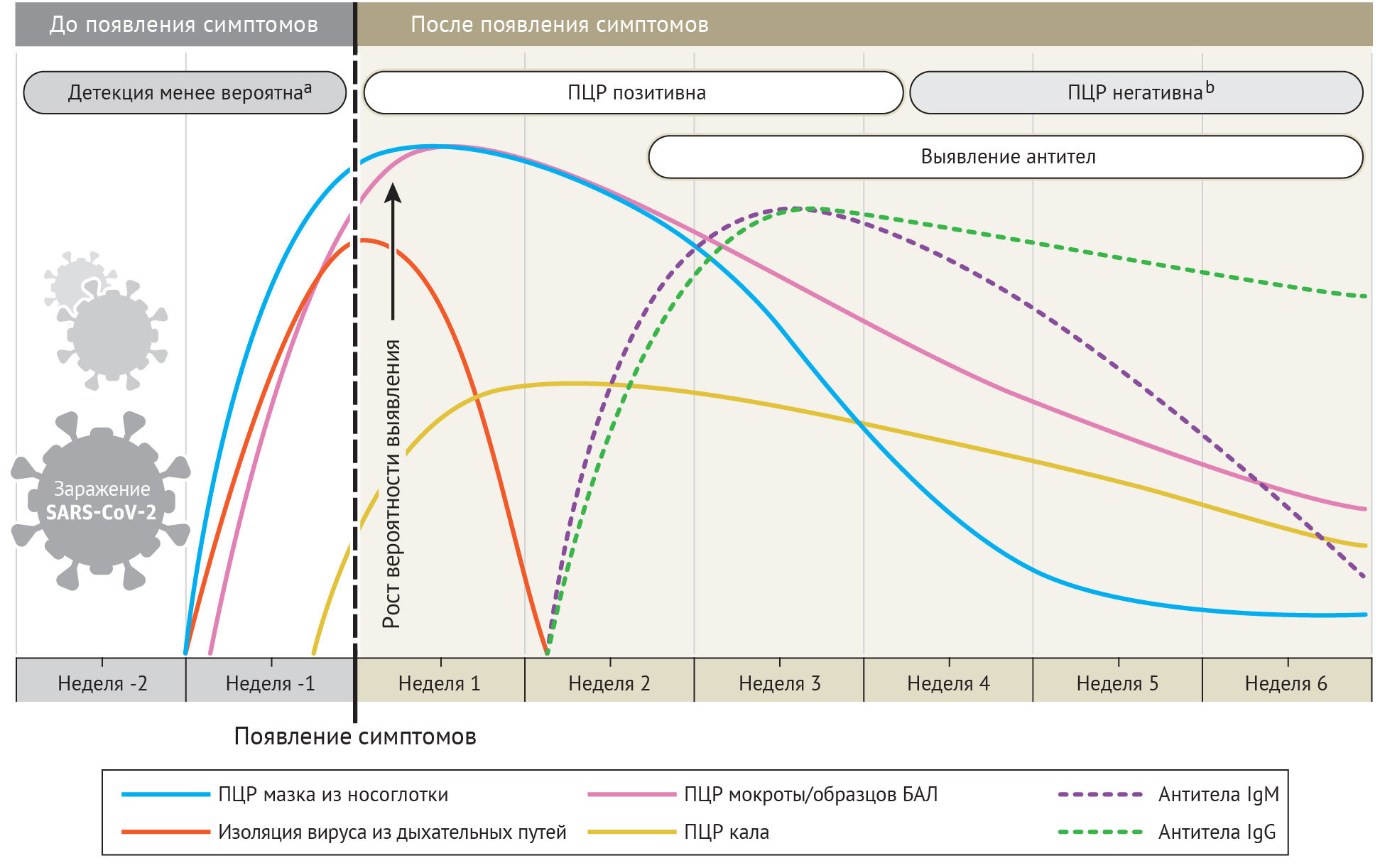
У большинства людей с симптомами коронавирусной инфекции нагрузка вирусной РНК в мазке из носоглотки определяется по порогу числа циклов (cycle treshold, Ct), выявляется со дня появления симптомов и становится максимальной в течение первой недели. Ct — это количество циклов репликации, необходимое для формирования флюоресцентного сигнала. При этом наименьший показатель Ct соответствует наибольшей нагрузке вирусной РНК. Показатель Ct менее, чем 40, клинически соответствует положительной ПЦР. Этот уровень начинает снижаться к третьей неделе заболевания и вскоре становится неопределяемым. Показатель Ct у госпитализированных пациентов с тяжелыми случаями инфекции ниже такового при легко протекающих формах; в тяжелых случаях положительная ПЦР может отмечаться более трех недель с момента начала заболевания, тогда как большинство легких случаев в это время будут показывать негативный результат. Как бы то ни было, положительная ПЦР отражает только присутствие вирусной РНК и не обязательно показывает наличие жизнеспособных вирусов.
В некоторых случаях вирусная РНК определяется методом ПЦР с обратной транскрипцией даже через шесть недель после первого позитивного теста. В нескольких случаях тест был положителен после двух последовательных негативных тестов ПЦР, проведенных с разницей в 24 часа. Неясно, было это обусловлено ошибкой в исследовании, реинфекцией или реактивацией. В исследовании девяти пациентов попытки изолировать вирус в культуре после восьмого дня с момента начала заболевания не увенчались успехом, что объясняется снижением инфекционных свойств вируса после первой недели. Отчасти поэтому «стратегия, основанная на симптомах» Центра по контролю и профилактике заболеваний показывает, что «медицинские работники могут приступить к работе, если как минимум три дня (72 часа) прошло с момента выздоровления: отсутствие лихорадки без применения антипиретиков и снижение респираторных симптомов (кашель, затруднение дыхания); и как минимум 10 дней прошло с того момента, как симптомы впервые появились».
Временная шкала изменения результатов ПЦР изменяется, если в качестве образцов используют не мазок из носоглотки. «Позитивность» ПЦР снижается медленнее в мокроте и может быть выявлена даже после того, как мазки из носоглотки уже отрицательны. В одном исследовании ПЦР была позитивна в образцах кала у 55 из 96 инфицированных пациентов (57 %) и оставалась позитивной после получения отрицательного результата в мазке из носоглотки с медианой 4–11 дней. При этом обнаружение позитивной ПЦР в кале не коррелировало с клинической тяжестью процесса. По оценкам Wolfel с соавт. длительность выявления положительной ПЦР в мокроте и кале одинакова.
В исследовании 205 пациентов с подтвержденной коронавирусной инфекцией вирусная нагрузка, выявленная ПЦР с обратной транскрипцией, была высокой в образцах, полученных методом бронхоальвеолярного лаважа (93 %), в мокроте (72 %), назофарингеальных мазках (63 %) и глоточных мазках (32 %). Ложноотрицательные результаты в основном появлялись при несоблюдении временного интервала забора образцов и нарушении техники забора, особенно в случае мазков из носоглотки. Специфичность большинства тестов ПЦР с обратной транскрипцией составляет 100 %, потому что дизайн праймеров высоко специфичен к геномной последовательности SARS-CoV-2. Случайные ложнопозитивные результаты могут появляться вследствие технических ошибок или контаминации образца.
Выявление антител к SARS-CoV-2
Инфицирование коронавирусом также может быть определено непрямым способом — путем исследования иммунного ответа пациента. Серологический диагноз особенно важен для пациентов с легкими или среднетяжелыми формами, которые могут начать наблюдаться поздно, по прошествии первых двух недель от начала заболевания. Серологический диагноз также становится важным инструментом для понимания степени распространения COVID-19 в популяции и выявления лиц, иммунизированных и «защищенных» от заражения.
Наиболее чувствительным и ранним серологическим маркером является общий уровень антител. Уровни IgM и IgG начинают нарастать со второй недели с момента появления симптомов; ИФА для их определения обычно становится положительным раньше, на четвертый день после появления симптомов, достигая максимального уровня на 2–3 недели заболевания.
Как было показано на 23 пациентах в исследовании To и соавт. и 85 пациентах в исследовании Xiang с соавт., сероконверсия IgM и IgG появляется у всех пациентов между третьей и четвертой неделями заболевания. К этому времени уровень IgM начинает снижаться, достигает наименьшего значения к 5 неделе и полностью исчезает к седьмой неделе, тогда как IgG выявляется позже седьмой недели. В исследовании 140 пациентов, чувствительность комбинации методов ПЦР и ИФА в отношении антигена нуклеокапсида (NC) составила 98,6 % в сравнении с таковой в 51,9 % у одной ПЦР. В течение первых 5,5 дней количественная ПЦР имеет более высокий рейтинг выявления положительных случаев, чем ИФА, затем этот показатель меняется.
ИФА для определения IgM и IgG имеет более чем 95 % специфичность для диагностики COVID-19. Первоначальная ПЦР, исследование парных сывороток и второе исследование через две недели могут повысить точность диагностики. Как правило, большинство антител продуцируются против наиболее интенсивно вырабатываемого протеина вируса — нуклеокапсида. Поэтому тесты, которые выявляют антитела к нуклеокапсиду, должны быть более чувствительными. С другой стороны, белок RBD-S — это белок прикрепления из организма хозяина, и исследование антител к нему должно быть более специфичным. Исследование одного или обоих антигенов для выявления IgG и IgM должно повысить общую чувствительность. Антитела могут, однако, показывать перекрестную реактивность в отношении SARS-CoV-2 и других коронавирусов.
Экспресс-тесты для детекции антител широко разрабатываются и продаются, имея при этом разный уровень качества. Многие производители не раскрывают природу используемых антигенов. Эти тесты редко показывают результат в качественном отношении; как правило, ими можно выявить только присутствие или отсутствие антител против SARS-CoV-2. Наличие нейтрализующих антител может показать только реакция нейтрализации, но высокие титры IgG в ИФА могут позитивно коррелировать с уровнем нейтрализующих антител. Длительность существование и функционирования нейтрализующих антител остается неизвестной.
Выводы
С использованием доступных доказательств была выработана клинически применимая временная шкала диагностических маркеров для детекции COVID-19. Большинство доступных сведений актуальны для взрослых не иммунокомпрометированных лиц. Время обнаружения положительной ПЦР и сероконверсии может изменяться у детей и некоторых групп взрослых, включая большое число бессимптомных пациентов, диагностика коронавирусной инфекции у которых требует активного вмешательства. Остается много вопросов, например, как долго сохраняется иммунитет у перенесших COVID-19 лиц с симптомами и без таковых.