Что такое химическая вакцина
Что такое химическая вакцина
Вакцины — иммунобиологические препараты, предназначенные для активной иммунопрофилактики, то есть для создания активной специфической невосприимчивости организма к конкретному возбудителю. Вакцинация признана ВОЗ идеальным методом профилактики инфекционных заболеваний человека. Высокая эффективность, простота, возможность широкого охвата вакцинируемых лиц с целью массового предупреждения заболевания вывели активную иммунопрофилактику в большинстве стран мира в разряд государственных приоритетов. Комплекс мероприятий по вакцинации включает отбор лиц, подлежащих вакцинации, выбор вакцинного препарата и определение схемы его использования, а также (при необходимости) контроль эффективности, купирование возможных патологических реакций и осложнений. В качестве Аг в вакцинных препаратах выступают:
• цельные микробные тела (живые или убитые);
• отдельные Аг микроорганизмов (наиболее часто протективные Аг);
• токсины микроорганизмов;
• искусственно созданные Аг микроорганизмов;
• Аг, полученные методами генной инженерии.
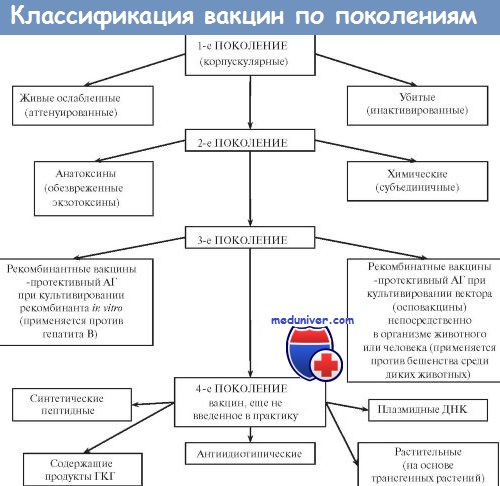
Большинство вакцин разделяют на живые, инактивированные (убитые, неживые), молекулярные (анатоксины) генно инженерные и химические; по наличию полного или неполного набора Аг — на корпускулярные и компонентные, а по способности вырабатывать невосприимчивость к одному или нескольким возбудителям — на моно- и ассоциированные.
Живые вакцины
Живые вакцины — препараты из аттенуированных (ослабленных) либо генетически изменённых патогенных микроорганизмов, а также близкородственных микробов, способных индуцировать невосприимчивость к патогенному виду (в последнем случае речь идёт о так называемых дивергентных вакцинах). Поскольку все живые вакцины содержат микробные тела, то их относят к группе корпускулярных вакцинных препаратов.
Иммунизация живой вакциной приводит к развитию вакцинального процесса, протекающего у большинства привитых без видимых клинических проявлений. Основное достоинство живых вакцин— полностью сохранённый набор Аг возбудителя, что обеспечивает развитие длительной невосприимчивости даже после однократной иммунизации. Живые вакцины обладают и рядом недостатков. Наиболее характерный — риск развития манифестной инфекции в результате снижения аттенуации вакцинного штамма. Подобные явления более типичны для противовирусных вакцин (например, живая полиомиелитная вакцина в редких случаях может вызвать полиомиелит вплоть до развития поражения спинного мозга и паралича).
Ослабленные ( аттенуированные ) вакцины
Ослабленные (аттенуированные) вакцины изготавливают из микроорганизмов с пониженной патогенностью, но выраженной иммуногенностью. Введение вакцинного штамма в организм имитирует инфекционный процесс: микроорганизм размножается, вызывая развитие иммунных реакций. Наиболее известны вакцины для профилактики сибирской язвы, бруцеллёза, Ку-лихорадки, брюшного тифа. Однако большая часть живых вакцин — противовирусные. Наиболее известны вакцина против возбудителя жёлтой лихорадки, противополи-омиелитная вакцина Сэйбина, вакцины против гриппа, кори, краснухи, паротита и аденовирусных инфекций.
Дивергентные вакцины
В качестве вакцинных штаммов используют микроорганизмы, находящиеся в близком родстве с возбудителями инфекционных болезней. Аг таких микроорганизмов индуцируют иммунный ответ, перекрёстно направленный на Аг возбудителя. Наиболее известны и длительно применяются вакцина против натуральной оспы (из вируса коровьей оспы) и БЦЖ для профилактики туберкулёза (из микобактерий бычьего туберкулёза).
Формы вакцинации
Формы вакцинации
Все вакцины подразделяются на живые и инактивированные. Инактивированные вакцины, в свою очередь, делят на:
Корпускулярные
— представляют собой бактерии или вирусы, инактивированные химическим (формалин, спирт, фенол) или физическим (тепло, ультрафиолетовое облучение) воздействием. Примерами корпускулярных вакцин являются: коклюшная (как компонент АКДС и Тетракок), антирабическая, лептоспирозная, гриппозные цельновирионные, вакцины против энцефалита, против гепатита А (Аваксим), инактивированная полиовакцина (Имовакс Полио, или как компонент вакцины Тетракок).
Химические
— создаются из антигенных компонентов, извлеченных из микробной клетки. Выделяют те антигены, которые определяют иммуногенные характеристики микроорганизма. К таким вакцинам относятся: полисахаридные вакцины (Менинго А+С, Акт-ХИБ, Пневмо 23, Тифим Ви), ацеллюлярные коклюшные вакцины.
Рекомбинантные
— для производства этих вакцин применяют рекомбинантную технологию, встраивая генетический материал микроорганизма в дрожжевые клетки, продуцирующие антиген. После культивирования дрожжей из них выделяют нужный антиген, очищают и готовят вакцину. Примером таких вакцин может служить вакцина против гепатита В (Эувакс В).
Инактивированные
вакцины выпускают как в сухом (лиофилизированном), так и в жидком виде.
Живые
Живые вакцины изготовляют на основе ослабленных штаммов микроорганизма со стойко закрепленной авирулентностью (безвредностью). Вакцинный штамм, после введения, размножается в организме привитого и вызывает вакцинальный инфекционный процесс. У большинства привитых вакцинальная инфекция протекает без выраженных клинических симптомов и приводит к формированию, как правило, стойкого иммунитета. Примером живых вакцин могут служить вакцины для профилактики краснухи (Рудивакс), кори (Рувакс), полиомиелита (Полио Сэбин Веро), туберкулеза, паротита (Имовакс Орейон).
Живые вакцины выпускаются в лиофилизированном (порошкообразном) виде (кроме полиомиелитной).
Анатоксины
Эти препараты представляют собой бактериальные токсины, обезвреженные воздействием формалина при повышенной температуре с последующей очисткой и концентрацией. Анатоксины сорбируют на различных минеральных адсорбентах, например на гидроокиси алюминия. Адсорбция значительно повышает иммуногенную активность анатоксинов. Это связано как с созданием «депо» препарата в месте введения, так и с адъювантным действием сорбента, вызывающего местное воспаление, усиление плазмоцитарной реакции в регионарных лимфатических узлах. Анатоксины обеспечивают развитие стойкой иммунологической памяти, этим объясняется возможность применения анатоксинов для экстренной активной профилактики дифтерии и столбняка.
В России производится около 40-ка видов вакцин. Среди них:
Уничтожение неиспользованных вакцин
Ампулы и другие емкости с неиспользованными остатками инактивированных бактериальных и вирусных вакцин, а также живой коревой, паротитной и краснушной вакцин, анатоксинов, иммуноглобулинов человека, гетерологичных сывороток, аллергенов, бактериофагов, эубиотиков, а также одноразовый инструментарий, который был использован для их введения не подлежит какой-либо специальной обработке.
Емкости, содержащие неиспользованные остатки других живых бактериальных и вирусных вакцин, а также инструментарий, использованный для их введения, подлежат кипячению в течение 60 минут (сибиреязвенная вакцина 2 ч), или обработке 3-5% раствором хлорамина в течение 1 ч, или 6% раствором перекиси водорода (срок хранения не более 7 сут) в течение 1 ч, или автоклавируются.
Все неиспользованные серии препаратов с истекшим сроком годности, а также не подлежащие применению по другим причинам следует направлять на уничтожение в районный (городской) центр санэпиднадзора.
Клещевой энцефалит
В природе основным переносчиком вируса клещевого энцефалита являются иксодовые клещи, ареал обитания которых находится по всей лесной и лесостепной умеренной климатической зоне Евразийского континента. Для клещевого энцефалита характерна строгая весенне-летняя сезонность, связанная с сезонной активностью переносчиков. Инфицирование человека вирусом клещевого энцефалита происходит во время присасывания энцефалитных клещей. Передача вируса клещевого энцефалита возможна и через желудочно-кишечный тракт при приёме сырого молока коз, зараженных клещевым энцефалитом.
Вы можете сделать прививку отечественной вакциной и вакциной ФСМЕ-ИММУН Инжект (пр-во Австрия).
Иммунизация отечественной вакциной состоит из 2х курсов внутримышечных инъекций по 1 дозе (0,5 мл) с интервалом в 7 месяцев. Курс вакцинации (2 прививки) можно проводить в течение всего года, в том числе и в летний период (эпидсезон), но не позднее, чем за 2 недели до посещения очага клещевого энцефалита. Наиболее оптимальным является интервал между 1-й и 2-й прививками 5-7 мес.(осень-весна). Ревакцинацию проводят 1 кратно в дозе 0,5 мл через 1 год после завершения курса вакцинации. Последующие отдаленные ревакцинации проводят каждые 3 года однократно.
Иммунизация вакциной ФСМЕ-ИММУН Инжект проходит в 3 этапа:
После введения вакцин, как отечественной, так и австрийской, в отдельных случаях могут развиваться местные и общие реакции. Местные реакции выражаются в покраснении, припухлости, болезненности в месте введения, развитии инфильтрата. Возможно небольшое увеличение регионарных лимфоузлов. Продолжительность местных реакций не превышает 3 суток. Общие реакции могут развиваться в первые 2 суток после вакцинации и выражаются в подъёме температуры, головной боли, недомогании, их продолжительность не превышает 48 часов. После второй вакцинации лихорадка наблюдается очень редко, может появляться кратковременная сыпь, сопровождаемая зудом (крайне редко).
Грипп – это вирусная инфекция,
Тяжесть болезни зависит от общего состояния организма, возраста (наиболее уязвимы дети, беременные женщины, люди пожилого возраста), бытовых условий (в плохо проветриваемых, пыльных помещениях создаются идеальные условия для размножения вируса гриппа). Вирус гриппа очень легко передается.
Вакцинацию лучше проводить осенью, поскольку эпидемии гриппа в классическом их варианте бывают между ноябрем и мартом. Высокий титр антител, вызванный прививкой, держится несколько месяцев и начинает снижаться спустя 6 месяцев после вакцинации.
В нашей клинике мы предлагаем всем желающим пройти вакцинацию против гриппа, либо вакциной «Инфлювак», Нидерланды, либо «Ваксигрип», Франция. Вакцина приводит к выработке иммунитета только против 3-х штаммов вируса гриппа, содержащихся в препарате, или против штаммов, сходных с указанными.
Принципиального отличия между этими вакцинами нет. Опыт применения вакцин у беременных женщин ограничен. Тем не менее, имеющийся опыт показывает, что данные вакцины не оказывают тератогенного или токсического действия на плод.
Вакцинацию можно проводить беременным женщинам, начиная со 2-го триместра беременности. Перед вакцинацией обязательно нужно посетить терапевта, который после осмотра, исключающего у вас наличие противопоказаний для вакцинации, порекомендует ту или иную вакцину.
Как разрабатывают вакцины?
Данная статья входит в серию публикаций, посвященных разработке и распределению вакцин. Узнайте больше о вакцинах, о принципах их действия и о том, как обеспечивается их безопасность и справедливое распределение, в серии публикаций ВОЗ «Все о вакцинах».
Какие ингредиенты входят в состав вакцины?
Вакцины содержат крошечные фрагменты болезнетворного микроорганизма или программы для создания этих крошечных фрагментов. Они также содержат другие ингредиенты, необходимые для обеспечения безопасности и эффективности вакцины. Эти последние ингредиенты включены в большинство вакцин и использовались на протяжении десятилетий в миллиардах доз вакцин.
Каждый компонент вакцины служит конкретной цели, и каждый ингредиент тестируется в процессе производства. Все ингредиенты тестируются на безопасность.
Антиген
Все вакцины содержат активный компонент (антиген), который генерирует иммунный ответ, или программу для создания активного компонента. Антиген может быть небольшой частью болезнетворного микроорганизма, такой как белок или сахар, или же это может быть весь микроорганизм в ослабленной или инактивированной форме.
Консерванты
Консерванты предотвращают контаминацию вакцины после открытия флакона, если она используется более чем для одного человека. Некоторые вакцины не имеют консервантов, поскольку они хранятся в однодозовых флаконах, которые выкидываются после введения одной дозы. Наиболее широко используемым консервантом является 2-феноксиэтанол, который используется в течение многих лет в ряде вакцин и ряде продуктов по уходу за младенцами. Этот консервант безопасен для использования в вакцинах, поскольку он мало токсичен для людей.
Стабилизаторы
Стабилизаторы предотвращают химические реакции внутри вакцины и удерживают компоненты вакцины от прилипания к флакону.
Стабилизаторы могут быть сахарами (лактозой, сахарозой), аминокислотами (глицином), желатином и белками (рекомбинантным человеческим альбумином, полученным из дрожжей).
Поверхностно-активные вещества
Поверхностно-активные вещества сохраняют все ингредиенты вакцины в смешанном состоянии. Они предотвращают образование осадка и склеивание элементов, находящихся в жидкой форме вакцины. Они также часто используются в пищевых продуктах, таких как мороженое.
Примеси
Примеси представляют собой крошечные количества различных веществ, используемых во время изготовления или производства вакцин, которые не являются активными ингредиентами готовой вакцины. Вещества варьируются в зависимости от используемого производственного процесса и могут включать яичные белки, дрожжи или антибиотики. Остаточные следы этих веществ, которые могут присутствовать в вакцине, находятся в столь малых количествах, что их необходимо измерять в частях на миллион или в частях на миллиард.
Разбавители
Разбавитель – это жидкость, используемая для разбавления вакцины до правильной концентрации непосредственно перед ее использованием. Чаще всего в качестве разбавителя используется стерильная вода.
Адъюванты
Некоторые вакцины содержат также адъюванты. Адъювант улучшает иммунную реакцию на вакцину иногда путем более длительного удержания вакцины в месте инъекции или стимулирования местных иммунных клеток.
Адъювантом может быть незначительное количество алюминиевых солей (например, фосфат алюминия, гидроксид алюминия или сульфат калия-алюминия). Было продемонстрировано, что алюминий не вызывает каких-либо долговременных проблем со здоровьем, и люди регулярно потребляют алюминий во время еды и питья.
Как разрабатывают вакцины?
Наиболее часто используемые вакцины применяются уже на протяжении десятилетий, и каждый год миллионы людей получают их, не подвергаясь при этом опасности. Как и все лекарственные средства, каждая вакцина должна пройти широкомасштабное тщательное тестирование для оценки ее безопасности, прежде чем она может быть включена в программу вакцинации в странах.
Каждая разрабатываемая вакцина должна сначала пройти проверки и оценки, помогающие определить, какой антиген следует использовать, чтобы вызвать иммунную реакцию. Эта доклиническая фаза испытаний проводится без участия людей. Экспериментальные вакцины сначала тестируются на животных для оценки их безопасности и способности предотвращать болезнь.
Если вакцина вызывает иммунную реакцию, она затем тестируется в рамках клинических испытаний с участием людей, которые состоят из трех фаз.
Фаза 1
Вакцина вводится небольшому числу добровольцев, чтобы оценить ее безопасность, убедиться, что она генерирует иммунную реакцию, и определить правильную дозу. Как правило, во время этой фазы испытаний вакцины тестируются на молодых взрослых добровольцах.
Фаза 2
Затем вакцина вводится сотням добровольцев для дальнейшей оценки ее безопасности и способности генерировать иммунную реакцию. Участники этой фазы испытаний обладают теми же характеристиками (такими как возраст и пол), что и люди, для которых предназначается вакцина. Обычно на этом этапе проводится несколько испытаний для оценки разных возрастных групп и разных составов вакцины. На этом этапе в испытания обычно включается группа, не получавшая вакцину, в качестве группы сравнения для определения того, относятся ли изменения, произошедшие в вакцинированной группе участников, к вакцине или же они произошли случайно.
Фаза 3
Затем вакцина вводится тысячам добровольцев, и проводится сравнение с аналогичной группой людей, которые не получали вакцину, но получали продукт сравнения, с целью определить, эффективна ли вакцина против болезни, для защиты от которой она предназначается, и изучить ее безопасность среди гораздо большего числа людей. Большую часть времени испытания на этом этапе проводятся в разных странах и в разных местах внутри стран, с тем чтобы удостовериться в том, что полученные результаты в отношении эффективности вакцины применимы к разным группам населения.
Во время испытаний второй и третьей фазы добровольцы и ученые, проводящие исследование, не знают, какие добровольцы получили испытываемую вакцину, а какие – продукт сравнения. Этот метод, называемый «ослеплением», необходим для обеспечения того, чтобы ни добровольцы, ни ученые не подвергались влиянию в своей оценке безопасности или эффективности в связи с тем, что знали, кто какой продукт получил. После завершения испытаний и получения всех результатов добровольцы и ученые-испытатели информируются о том, кто получил вакцину, а кто – продукт сравнения.
После получения результатов всех этих клинических испытаний необходимо предпринять ряд шагов, включая проведение обзоров эффективности и безопасности для утверждения нормативных актов и политики в области общественного здравоохранения. Должностные лица в каждой стране внимательно изучают данные исследования и принимают решение о том, следует ли санкционировать использование вакцины. Вакцина должна быть признана безопасной и эффективной для широких слоев населения, прежде чем она будет утверждена и включена в национальную программу иммунизации. Уровень безопасности и эффективности вакцин чрезвычайно высок при том понимании, что они вводятся людям, которые здоровы и, в частности, не имеют той болезни, для защиты от которой они предназначаются.
После внедрения вакцины проводится постоянный мониторинг. Существуют системы для мониторинга безопасности и эффективности всех вакцин. Это позволяет ученым отслеживать воздействие вакцин и их безопасность, даже если они используются среди большого числа людей в течение длительного времени. Эти данные используются для корректировки политики в отношении использования вакцин в целях оптимизации их воздействия и для безопасного отслеживания воздействия вакцины во время ее использования.
Как только вакцина начинает применяться, необходимо проводить постоянный мониторинг для удостоверения в том, что она остается безопасной.
Чем на самом деле является вакцина от коронавируса? Испытания, скрытые компоненты и правда о сроках разработки «Спутник V»
Чем на самом деле является вакцина от коронавируса? Испытания, скрытые компоненты и правда о сроках разработки «Спутник V»

Институт им. Гамалеи, где и был синтезирован «Спутник V», создавал вакцины на основе аденовируса с 2015 г., поэтому ученым в относительно небольшие сроки удалось создать вакцину от коронавируса. Она защищает организм от заражения следующим образом: в аденовирусный вектор (вирус), который искусственно лишили возможности размножаться, вшили ген, кодирующий S-белок шипа коронавируса. Вектор доставляет кусочек РНК-вируса в клетку, а та, в свою очередь, реагирует на это так же, как реагировала бы на вторжение SARS-CoV-2. Начинают вырабатываться специфические антитела, которые и создают иммунитет против коронавируса.
Что входит в состав вакцины от коронавируса и содержатся ли в ней опасные «ингредиенты»?
Аденовирусный вектор – основное действующее вещество вакцины. Это главное составляющее, но, для работы прививки необходимы и другие компоненты. Они помогают сохранить эффект действующего вещества и облегчают его проникновение в клетки человека.
Помимо самого аденовирусного вектора в состав «Спутник V» входят:
Каждый «ингредиент» прививки от коронавируса абсолютно безвреден. Для того чтобы проверить, формируют ли в связке все эти компоненты устойчивый иммунитет к коронавирусу, проводятся испытания.
Какие испытания прошла вакцина от коронавируса?
Сразу после синтеза нового препарата, ученые провели доклиническое тестирование на хомячках и приматах. Проверяли токсичность, безопасность и эффективность новой вакцины. Никаких осложнений, побочных реакций у животных не возникло, поэтому ученые приступили к клиническим испытаниям на людях.
Первая фаза испытаний обычно проводится на небольшой группе здоровых добровольцев. Для тестирования российской вакцины «Спутник V» было привлечено 76 военных возрастом от 18 до 60 лет. Фаза была разделена на два этапа.
Первый этап длился 28 дней. Девятнадцати добровольцам поставили первую часть вакцины, основанной на ослабленном аденовирусе 26 типа, другим девятнадцати – вторую, с аденовирусом 5 типа. Так была проверена безопасность обоих компонентов вакцины. Результатом этапа стала хорошая переносимость препарата всеми добровольцами. Побочные эффекты были легкими или умеренными:
Опасных для жизни побочных эффектов обнаружено не было.
Во время второго этапа исследовался уже формирующийся после вакцинации иммунитет. Все добровольцы получили обе части вакцины с разницей в 21 день между ними. На 28 день после введения второй дозы, с помощью высокоточных тестов, у 100% добровольцев были обнаружены антитела к SARS-CoV-2. Более того, было доказано формирование другого – клеточного иммунитета. Обычно он сохраняется в «памяти» организма несколько лет.
Спустя три месяца после старта третьей фазы клинических испытаний в декабре 2020 г. российский Минздрав принял решение совместить последний этап исследований с массовой вакцинацией населения прививкой «Спутник V». Решение приняли оперативно, основываясь на предварительных результатах, опубликованных разработчиками вакцины в ноябре 2020 г.
В основе проведенных расчетов лежат случаи заболевания COVID-19 среди уже привитых добровольцев. Из общего числа участников испытаний, получивших обе положенные инъекции вакцины или плацебо (18 794), к концу третьей недели после второго укола вирус был диагностирован у 39 человек.
31 случай заражения был выявлен у тех, кто получил плацебо. В группе волонтеров, привитых настоящей вакциной, COVID-19 был диагностирован у восьмерых (группа получивших вакцину – в три раза больше группы плацебо). Сопоставление результатов по двум группам дает результат эффективности вакцины в 95%.
«Набранная группа участников исследований позволяет в полной мере исследовать профиль безопасности и профилактической эффективности вакцины на длительном промежутке времени», – пояснили в Минздраве.
Несмотря на то, что прививка «Спутник V» стала доступна всем желающим (за исключением группы с противопоказаниями), ученые продолжили наблюдение за добровольцами, принявшими участие в третьей фазе клинических испытаний. Второго февраля 2021г. разработчики вакцины представили результаты исследования в авторитетном медицинском издании The Lancet.
Результаты последней третьей фазы клинических испытаний вакцины «Спутник V»
Третья фаза испытаний вакцины «Спутник V» длилась с 7 сентября по 24 ноября. В ней приняли участие 21 977 человек, из них 16 427 были привиты, а 5435 – получили плацебо (раствором, в который входят все ингредиенты «Спутник V», кроме самого аденовирусного вектора).
Согласно выводам ученых специфические антитела против коронавируса вырабатывались через 42 дня после первой прививки или через 21 день после второй у 95,8% добровольцев. Более того, в день первой инъекции и через 28 дней после второй у добровольцев уже определялся клеточный иммунитет.
Что касается побочных эффектов, они проявились у 7966 привитых, при этом у 94% из них были легкими и включали повышение температуры, неприятные ощущения в месте инъекции, головную боль и слабость. Лишь 0,3% привитых имели серьезные побочные эффекты, однако, независимая комиссия не доказала связи между ними и вакцинацией.
Эффективность вакцины при таких показателях составляет 91.6%.
«Спутник V» также исследовали на добровольцах старше 60 лет – всего 2144 человека. Эффективность вакцины в этой группе практически не отличается от общей и составляет 91.8%.
Таким образом, вакцина показала свою эффективность и безопасность как у людей от 18 до 60 лет, так и у пожилых добровольцев. При этом серьезных побочных эффектов, связанных с вакциной, обнаружено не было.
Быстро не значит плохо: почему вакцину от коронавируса разработали за короткие сроки?
Разработка и тестирование вакцины заняли около года. Это уникальный, но объяснимый, случай. Прежде всего, ускорило создание «Спутник V» то, что вакцина была сделана на основе аденовирусного вектора. Такая технология уже давно известна ученым, а сам центр им. Гамалеи имел опыт в выпуске подобных вакцин. Ранее была разработана вакцина от ближневосточного респираторного синдрома. Вирус, который его вызывает – MERS, также относится к группе коронавирусов.
Быстрое распространение и способность к мутации вируса требовали кардинальных решений. При этом безопасность и эффективность вакцины на первом месте. Именно поэтому первые фазы исследования были проведены с соблюдением всех международных правил: количество добровольцев на каждой фазе, критерии оценки их состояния здоровья после вакцинации. Только после того, как вакцина показала свою безопасность и способность защищать от коронавируса, было принято решение о массовой вакцинации.
Как изменится мир после массовой вакцинации?
Идея коллективного иммунитета заключается в том, что, когда достаточно большое число людей в популяции уже обладает иммунитетом, инфекция лишается каналов распространения. Из-за этого вспышки заболевания быстро сходят на нет. Добиться коллективного иммунитета против коронавируса можно только путем вакцинации.
После массовой вакцинации будет снижена нагрузка на медицинский персонал и больницы, многие люди, особенно те, которые находятся в группе риска, смогут вернуться к привычной жизни. Вакцинация не только положит конец пандемии, но и поможет не бояться новых вспышек коронавируса.