что такое биуретовая реакция белков
Химия. 10 класс
§ 48. Белки
Белки
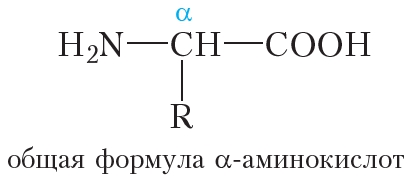
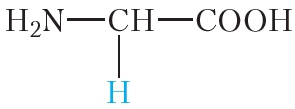
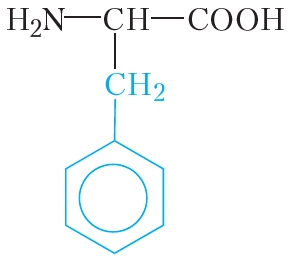
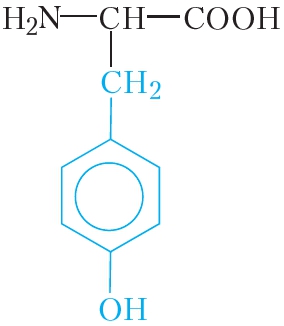
Молекулы белков построены из остатков α-аминокислот:
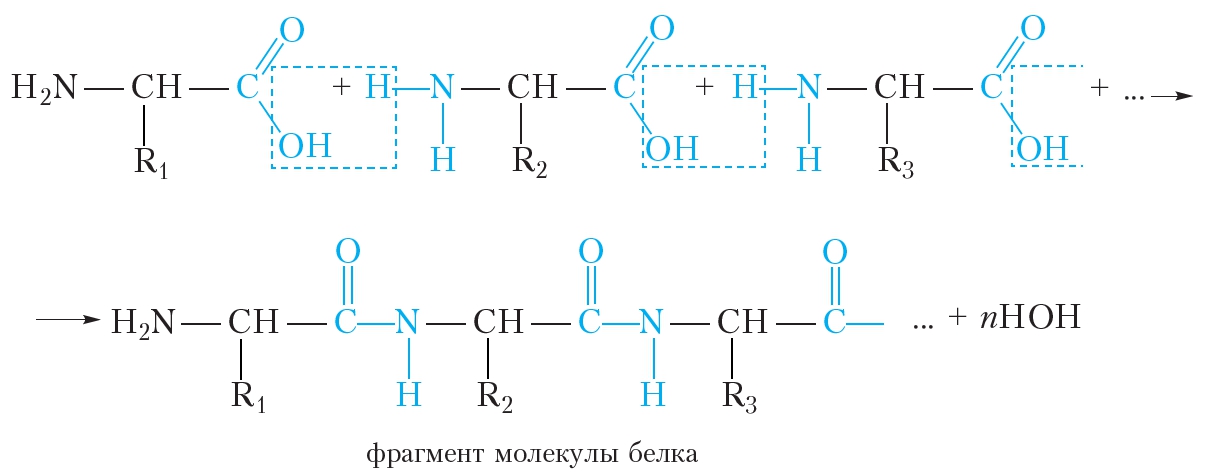
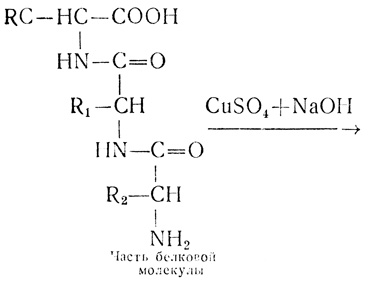
Образование молекулы белка из α-аминокислот можно представить следующей схемой:
Видно, что в молекулах белков аминокислотные остатки соединены пептидными связями, следовательно, белки являются полипептидами.
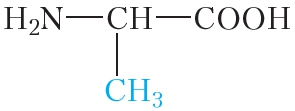
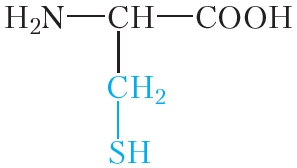
Молекулы белков обычно содержат сотни и даже тысячи аминокислотных остатков. При этом наиболее часто в составе белков встречаются остатки 20 разных аминокислот (табл. 48.1).
Таблица 48.1. Некоторые аминокислоты, остатки которых входят в состав белков

Остатки этих аминокислот расположены в макромолекуле белка в строго определённой последовательности (рис. 48.1).

На первый взгляд может показаться, что использование 20 разных аминокислот для построения молекул белков существенно ограничивает разнообразие белковых структур. На самом деле количество комбинаций, которое можно составить, используя для построения полипептидных цепей 20 разных аминокислот, практически бесконечно. Например, если полипептидная цепь будет состоять из 100 аминокислотных остатков, то, используя для её построения 20 различных аминокислот, можно составить 20 100 комбинаций!
Что такое биуретовая реакция белков
Биуретовая реакция
Биуретовая реакция служит для обнаружения пептидных связей. Пептидная связь наиболее характерна для белков, и в этом смысле биуретовая реакция являемся наиболее специфичной. В белках возможны и другие связи, например, сульфидная, эфирная, солевая, водородная. Для обнаружения этих связей биуретовая реакция негодна.
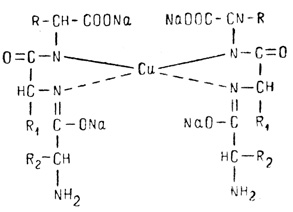
Биуретовая реакция основана на том, что в щелочной среде (в присутствии гидроокиси натрия) при добавлении солей меди (медного купороса) полипептиды и белки образуют окрашенные комплексные соединения с ионом меди.
Хотя отдельные аминокислоты этой реакции не дают, но, как исключение, она возникает в присутствии аспарагина и гистидина.
Отрицательной чертой биуретовой реакции является то, что она малочувствительна. Окрашивание особенно хорошо проявляется только там, где белков много (например, в меристематических клетках).
Проведение биуретовой реакции на свежем материале может дать ослабленное окрашивание из-за слабой проницаемости тканей. Фиксированный материал дает в этом отношении лучшие результаты; однако надо иметь в виду, что фиксация спиртом неприемлема для спирторастворимых белков (как, например, белки зерновых злаков).
1) 7%-ный раствор медного купороса.
2) 30-50%-ный раствор гидроокиси натрия (или калия).
1. Погрузить срез в раствор медного купороса на 5-30 мин в часовом стекле.
2. Тщательно отсосать этот раствор фильтровальной бумагой и промыть срез водой до удаления голубой окраски из промывной воды.
3. Перенести срез на предметное стекло и обработать раствором гидроокиси натрия (или калия) от 10-20 мин до 1 ч.
4. Наблюдать появление фиолетовой окраски (иногда розовой в присутствии низкомолекулярных белков или полипептидов).
Результаты реакции (табл. 17)
Реакция не идет в паренхиме листа капусты и проявляется неярко в тканях пучка.
Эндосперм зерновки кукурузы не дает реакции, не считая алейронового слоя, где она проявляется, хотя и очень незначительно. Зародыш окрашивается ярко.