что лучше таурин или лецитин
Таурин в лечении неалкогольной жировой болезни печени
Л. А. Звенигородская, Т. В. Нилова
Московский клинический научно-практический центр Проведено двойное слепое плацебоконтролируемое клиническое исследование, в котором оценивалась клиническая эффективность таурина у больных с неалкогольной жировой болезнью печени (НАЖБП) и сахарным диабетом типа 2 (СД2).
Результаты показали, что препарат влияет на обмен липидов и углеводов, а также является типичным гепатопротектором.
Ключевые слова: неалкогольная жировая болезнь печени, таурин, комплексное медикаментозное лечение
Taurine in non-alcoholic fatty liver disease treatment
L. A. Zvenigorodskaya, T. V. Nilova
Moscow Clinical Scientific and Practical Center In double-blind, placebo-controlled clinical trial taurine clinical efficacy in patients with non-alcoholic fatty liver disease and diabetes mellitus type 2 was evaluated.
The results of this study have shown effects of taurine on lipid and carbohydrate metabolism and also that taurine is a typical hepatoprotector.
Key words: non-alcoholic fatty liver disease, taurine, complex conservative prevention
Патогенез неалкогольной жировой болезни печени. Подходы к лечению
Неалкогольная жировая болезнь печени (НАЖБП) в настоящее время признана самым распространенным в популяции заболеванием и представляет собой поражение печени, включающее жировую дистрофию с воспалением и повреждением гепатоцитов – неалкогольным стеатогепатитом (НАСГ) и фиброзом с возможностью перехода в цирроз. НАЖБП в 75 % случаев протекает на фоне ожирения, дислипидемии, артериальной гипертонии, сахарного диабета типа 2 (СД2) или нарушением толерантности к глюкозе [1–3]. Указанные патологические процессы являются факторами риска сердечно-сосудистых заболеваний и атеросклероза. В патогенезе немаловажную роль играет нарушение микрофлоры толстой кишки и, как следствие, повышение содержания продуктов жизнедеятельности микроорганизмов (короткоцепочечные жирные кислоты, эндотоксин, оксид азота) [4–6]. Биопсия печени – наиболее специфичный и чувствительный диагностический метод выявления заболевания; когда нет возможности провести пункционную биопсию печени, для раннего выявления воспаления при НАЖБП можно использовать определение маркеров воспаления – оксида азота и эндотоксина [7].
В настоящее время для лечения больных НАЖБП используют препараты, сочетающие в себе антиоксидантную защиту, стабилизацию мембран гепатоцитов, противовоспалительную терапию [8].
Терапия НАЖБП включает следующие группы препаратов:
Надо отметить, что в терапии НАЖБП недооцененным остается таурин. Между тем, представляя собой естественный метаболит, таурин обладает гепатопротекторным, антиоксидантным, гиполипидемическим и гипогликемическим эффектами.
Общие сведения
Таурин – жизненно необходимая сульфоаминокислота, являющаяся конечным продуктом обмена серосодержащих аминокислот (метионина, цистеина, цистеамина) [9, 10]. Молекула таурина состоит из 2 атомов углерода, сульфоновой группы (SO3H) и аминогруппы (NH2). Биологический синтез таурина недостаточен для поддержания у человека тех биохимических процессов, в которых он задействован. Основным источником таурина являются мясные и рыбные продукты. При дефиците таурина в питании или в результате каких?либо иных причин (ишемия, сахарный диабет, стресс, травма и др.) страдают все виды обмена веществ любой клетки любого органа. Например, недостаточность таурина в печени ведет к нарушению желчевыделения, образованию камней, изменению обмена холестерина и липидов. Известно, что таурин, соединяясь с холевой кислотой, участвует во всасывании жиров и жирорастворимых витаминов.
Таурин может соединяться с атомом хлора, источник которого – гипохлорная кислота нейтрофилов. В этом виде таурин служит окислителем и является компонентом в борьбе против бактериальной инфекции. В митохондриях хлораминотаурин влияет на сборку белков дыхательной цепи и проявляет свойства антиоксиданта. Это же соединение таурина с хлором уменьшает воспалительный сигнал в клетках животных через ингибирование активации нуклеарного фактора k-би. В свободном виде таурин также выполняет жизненно важные для животной клетки функции – регуляцию осмотического давления и ионов кальция.
Роль таурина в физиологии печени
Таурин участвует в регуляции желчевыделения. Как мы помним, первичные желчные кислоты (холевая и хенодезоксихолевая) синтезируются в гепатоцитах печени из холестерина. Вторичные желчные кислоты (дезоксихолевая, литохолевая, урсодезоксихолевая, аллохолевая и др.) образуются из первичных желчных кислот в толстой кишке. В желчи желчного пузыря желчные кислоты присутствуют главным образом в виде конъюгатов – парных соединений с глицином и таурином. Продуктом конъюгации желчных кислот с таурином являются таурохолевая, таурохенодезоксихолевая и тауродезоксихолевая кислоты. Конъюгация желчных кислот обеспечивает их устойчивость в отношении выпадения в осадок при низких значениях рН в желчных протоках и двенадцатиперстной кишке. Важнейшая роль желчных кислот в пищеварении заключается в том, что с их помощью происходит всасывание целого ряда гидрофобных веществ: холестерина, жиров, жирорастворимых витаминов, растительных стероидов. При отсутствии желчных кислот всасывание вышеперечисленных компонентов пищи практически невозможно.
Поступление в кишечник таурохолевой кислоты снижает количество E. coli в слепой кишке [11]. Кроме того, тауроконъюгаты желчных кислот обладают холеретическим действием и предупреждают холестаз в отличие от желчных кислот, конъюгированных с глицином [12, 13]. В эксперименте in vitro гликолитохолевая кислота легко осаждается кальцием, чего не наблюдается с тауролитохолевой кислотой [14]. Таким образом, таурин необходим для повышения текучести желчи, увеличения продукции желчных кислот и предупреждения холестаза [15, 16].
При диффузных заболеваниях печени таурин увеличивает кровоток, улучшает микроциркуляцию и уменьшает выраженность цитолиза [1]. Показана его эффективность в отношении влияния на углеводный и липидный обмен. Антиоксидантное, гипогликемирующее, детоксицирующее действие таурина и его способность к выведению холестерина дает возможность применять его для лечения НАЖБП. На фоне приема таурина при хронической сердечной недостаточности больные отмечают исчезновение одышки, чувствуют прилив сил, увеличение трудоспособности, улучшение общего состояния. У больных с артериальной гипертонией препарат умеренно снижает артериальное давление (АД), при сахарном диабете (CД) уменьшает инсулинорезистентность, защищает b-клетки поджелудочной железы, оказывает гипогликемическое действие, не вызывая при этом гипогликемии.
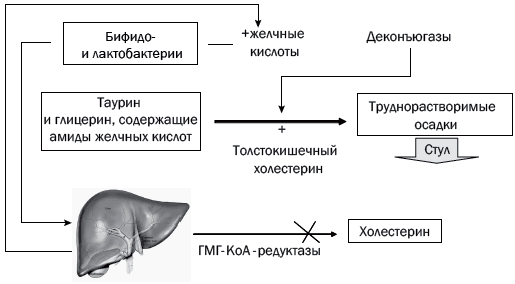
Рис. 1. Схема выведения холестерина
Взаимодействие желчных кислот и энтеробактерий
В процессах деконъюгации комплексов желчных кислот с таурином и глицином активно участвуют ферменты различных бактерий. В норме дезоксихолевая и хенодезоксихолевая кислоты при участии секреторного IgA, влияющего на антимикробную активность этих кислот, подавляют рост патогенных и условно-патогенных микроорганизмов даже в физиологических концентрациях [18]. При нарушении энтерогепатической циркуляции желчных кислот создается их значительный дефицит в кишечнике. В тонкой кишке недостаток желчных кислот изменяет работу всего пищеварительно-транспортного конвейера, способствует развитию нарушений всасывания и переваривания пищи – синдрома нарушенного пищеварения. В толстой кишке нехватка желчных кислот (помимо многочисленных метаболических нарушений) приводит к снижению «стерилизующих» и нутритивных свойств желчи. В результате – прогрессирование дисбиоза в толстой кишке, брожение, дисфункция баугиниевой заслонки и усиление микробной контаминации тонкой (подвздошной) кишки, с одной стороны, с другой – поступление через систему воротной вены с кровью в печень повышенного количества эндотоксина грамотрицательной микрофлоры. Важным и крайне необходимым условием восстановления энтерогепатической циркуляции желчных кислот является нормализация процессов синтеза желчи в печени и адекватного поступления ее в кишечник (табл. 1) [19]. Желчегонные свойства таурина в связи с этим также могут оказывать дополнительный эффект при лечении НАЖБП.
Таблица 1. Показатели обмена веществ у пациентов до начала исследования
| Показатель | Значение нормы | Первая группа, принимавшая таурин | Вторая группа, принимавшая плацебо |
| Белок | 66–87 г/л | 73,69±1,19 | 74,10±1,33 |
| Билирубин | 3,4–21 мкмоль/л | 15,39±1,84 | 18,14±1,98 |
| Глюкоза | 4,1–6,4 ммоль/л | 7,33±0,45 | 7,14±0,36 |
| АЛТ | 5–34 Ед/л | 51,48±8,90 | 37,33±10,84 |
| АСТ | 5–31 Ед/л | 39,13±6,53 | 31,67±5,47 |
| ЩФ (щелочная фосфатаза) | 30–120 Ед/л | 80,70±4,7 | 79,50±5,26 |
| ГГТП | 7–38 Ед/л | 67,86±17,56 | 52,91±6,35 |
| Мочевина | 1,7–8,3 ммоль/л | 5,22±0,39 | 5,23±0,47 |
| Холестерин | 1,4–5,2 мкмоль/л | 7,27±0,33 | 6,18±0,27 |
| ХС-ЛПНП | 2,1–3,3 мкмоль/л | 4,70±0,23 | 3,97±0,26 |
| ХС-ЛПВП | 1,1–2,3 ммоль/л | 1,37±0,12 | 1,27±0,10 |
| ТГ | 0,0–1,7 мкмоль/л | 2,43±0,21 | 2,01±0,09 |
| СРБ | мг/л | 7,23±0,30 | 7,56±0,50 |
Целью исследования было изучение фармакодинамических показателей метаболитов оксида азота (NO) и бактериального эндотоксина в результате трехмесячного курса фармакотерапии таурином у больных НАЖБП и СД2, сопоставление содержания оксида азота и эндотоксина у больных НАЖБП с СД2 с биохимическими показателями крови.
Материал и методы
В двойное слепое плацебо-контролируемое исследование было включено 40 больных, страдающих НАЖБП и СД2 (30 женщин и 10 мужчин), средний возраст которых составил 56,35±8,75 года. Верификацию диагноза проводили по данным клинических, биохимических, инструментальных методов исследования. Индекс массы тела больных был увеличен на 30–35 %, у некоторых – до 40 %. Все больные получали терапию по поводу сахарного диабета метформина гидрохлоридом, по поводу артериальной гипертензии – амлодипином и эналаприлом. Методом случайных чисел пациентов разделили на 2 группы. 1-я группа получала таурин (Дибикор, ООО «ПИК-ФАРМА») в дозе 0,5 г 2 раза в день за 20 мин до еды в течение 3 мес. 2-я, контрольная, группа дополнительно к основному лечению получала плацебо-таурин.
Уровень метаболитов оксида азота в сыворотке крови определяли экспресс-методом для биологических жидкостей с использованием ванадия хлорида (Германия) [20]. Уровень эндотоксина определяли ЛАЛ-тестом (США). Статистическую обработку данных проводили с использованием программы «Биостат».
Результаты
У больных НАЖБП отмечено повышение аминотрансфераз АЛТ и АСТ, а также гамма-глютамилтранспептидазы (ГГТП) у 35 больных. По показателям липидного спектра у обследованных больных также наблюдалось повышенное содержание общего холестерина, холестерина ЛПНП и триглицеридов (см. табл. 1). Как видно из таблицы, по некоторым показателям группы отличались. Повышение АСТ и АЛТ, а также общего холестерина и триглицеридов было более выражено в 1-й группе, билирубина и С-реактивного белка (СРБ) – во 2-й. По данным УЗИ выявлена жировая дистрофия печени у всех больных.
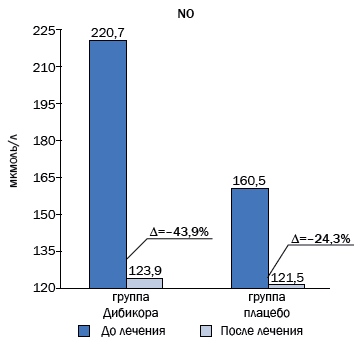
Уровень метаболитов оксида азота в 1-й группе до лечения был увеличен в 6,8 раза и составлял 220,70±14,27 мкмоль/л. Норма – 32,15±0,51 мкмоль/л (p=0,001). Во 2-й группе, получавшей плацебо, уровень метаболитов был несколько ниже, составил 160,50±8,87 мкмоль/л и был увеличен в 5 раз. В результате фармакотерапии таурином содержание метаболитов снизилось на 44 %, или на 97 мкмоль/л. В группе контроля (плацебо) снижение метаболитов оксида азота составило 25 %, или 39 мкмоль/л.
У больных НАЖБП уровень эндотоксина был увеличен в 7 раз (n=34) (норма – 0,29±0,05 Е/Эмл) и составлял 2,20±0,04 Е/Эмл. В результате проведения курса лечения с включением таурина содержание эндотоксина снизилось до 0,90±0,01 Е/Эмл (p=0,001). В группе плацебо (вторая группа) изменения были также статистически значимы, уровень эндотоксина достиг 1,80±0,05 Е/Эмл. Фармакотерапия больных НАЖБП с включением таурина снижает активность маркеров воспаления.
Достоверное увеличение продукции сывороточного эндотоксина сопровождалось ростом синтеза оксида азота и находилось в прямой корреляционной зависимости (коэффициент корреляции равен 0,625.) Лечение таурином сопровождалось улучшением биохимических показателей крови, улучшением общего самочувствия больных. Уровень метаболитов оксида азота снижался параллельно уровню АЛТ, АСТ и ГГТП. Изменения показателей обмена веществ приведены в табл. 2.
Таблица 2. Изменения показателей обмена веществ после курса лечения в группах таурина и плацебо, %
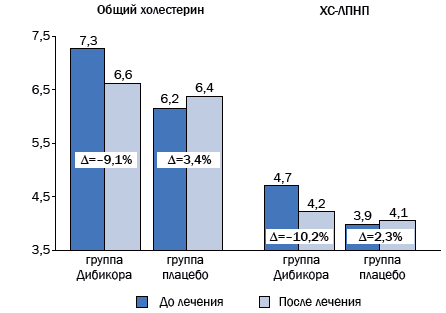
При данной выборке пациентов достоверно статистические изменения (снижение) наблюдали в 1-й группе по показателям АСТ, АЛТ, ГГТП. Остальные изменения были недостоверны. Наблюдалось достоверное снижение веса с 91,32±3,5 до 87,42±3,06; p=0,001. Во 2-й группе наблюдалась тенденция ухудшения – возрастание ЩФ, уровня гликемии, общего холестерина, ХС-ЛПНП. В 1-й группе ХСЛПВП не изменился, во 2-й – вырос на 17,3 %.
Рис. 2. Снижение уровня метаболитов NO на фоне фармакотерапии таурином и плацебо
Рис. 3. Динамика липидного спектра крови после 3-месячного курса терапии таурином
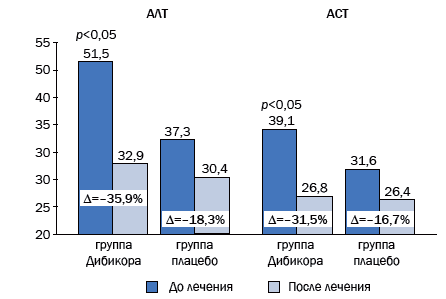
Рис. 4. Динамика показателей биохимического анализа крови у больных, получавших таурин
Обсуждение
Показано, что в 1-й и 2-й группах после лечения наблюдаются положительные изменения со стороны печеночных ферментов. Присоединение к терапии НАЖБП препарата Дибикор (таурин) способствует более выраженному уменьшению активности ферментов печени: АСТ (p
Литература
Целесообразность применения таурина в лечении неалкогольной жировой болезни печени
К.м.н. О.Н. ОВСЯННИКОВА, д.м.н., проф. Л.А. ЗВЕНИГОРОДСКАЯ
ЦНИИ гастроэнтерологии, Москва
Проведено двойное слепое плацебоконтролируемое сравнительное клиническое исследование, в котором оценивалась клиническая эффективность таурина (препарат Дибикор, производитель «ПИК-ФАРМА») у больных с неалкогольной жировой болезнью печени (НАЖБП) и сахарным диабетом 2 типа (СД 2 типа) в сравнении с плацебо. Результаты показали, что применение препарата Дибикор оказывает гиполипидемический и гепатопротективный эффект, улучшает показатели углеводного и жирового обмена, способствует снижению массы тела, улучшению самочувствия больных и может быть рекомендовано для коррекции и профилактики метаболических нарушений в терапии НАЖБП.
Впоследние годы неалкогольную жировую болезнь печени (НАЖБП) рассматривают как неотъемлемый компонент метаболического синдрома (МС). МС представляет собой комплекс связанных между собой факторов, включащих инсу-линорезистентность, нарушение углеводного обмена, абдоминально-висцеральное ожирение, артериальную гипертензию, ате-рогенную дислипидемию и др. Печень при МС является одним из основных органов-мишеней [1, 2]. Согласно данным ряда источников, частота патологии печени у больных с МС составляет от 37 до 64%.
НАЖБП: этиология, патогенез, задачи терапии
К этиологическим факторам развития НАЖБП относятся метаболические расстройства и эндокринопатии (инсулинорезистентность или СД, ожирение, подагра, гиперлипидемия, гипотиреоз, гипертиреоз, синдром Кушинга и др.); нарушение процессов пищеварения и всасывания (патология поджелудочной железы, тонкой кишки, синдром нарушенного всасывания, избыточное питание, голодание, парентеральное питание, синдром избыточного бактериального роста в кишечнике); действие лекарств, химических субстанций, фитотоксинов, токсинов грибов; инфекции; анемия, сердечно-сосудистая и дыхательная недостаточность и др. [3, 4]. НАЖБП имеет несколько стадий развития: от простого стеатоза до стеатогепатита, фиброза и цирроза печени. Симптомы, свойственные заболеваниям печени, отсутствуют у большинства больных, только некоторые из них отмечают незначительный дискомфорт или боль в правом верхнем квадранте живота [1]. У большей части пациентов НАЖБП протекает благоприятно, без значительных клинико-морфологических изменений. Поскольку возможность проведения пункции печени имеется далеко не всегда, истинная распространенность этого заболевания в популяции неизвестна. Чаще больные обращаются к врачам по другим причинам, например по поводу артериальной гипертонии (АГ), желчнокаменной болезни, ишемической болезни сердца (ИБС), заболеваний периферических сосудов и др. [5, 6]. В связи с этим лечение назначается только больным с высоким риском прогрессирования НАЖБП или при наличии выраженных изменений биохимических показателей печени (повышение активности алани-наминотрансаминазы (АЛТ) и ас-партатаминотрансаминазы (АСТ) в крови в 2-3 раза и более).
МС обусловливает чрезвычайно высокий риск развития СД 2 типа, ИБС и других заболеваний, связанных с атеросклерозом 8, а также жировой болезни печени [2]. Среди механизмов поражения печени необходимо выделить нарушение синтеза и экскреции желчи в гепатоцитах, активацию перекисного окисления липидов (ПОЛ), угнетение активности ретикуло-эндотели-альной системы печени. В литературе представлены многочисленные данные о возможных патогенетических механизмах повреждения печени при МС, а также о роли печени в развитии и прогрессировании МС. Печень является единственным органом, где осуществляется синтез желчных кислот. Накопление в печени свободных жирных кислот приводит к нарушению проницаемости клеточных мембран, в том числе для глюкозы, к нарушению утилизации глюкозы гепатоцитами, что способствует повышению резистентности тканей к инсулину и поддержанию гипергликемии. В условиях инсулинорезистент-ности происходит накопление ли-пидов в печени и синтез большого количества липопротеидов очень низкой плотности (ЛПОНП), которые быстро модифицируются в липопротеиды низкой плотности (ЛПНП) и, окисляясь под действием свободных радикалов, являются ведущим фактором развития атеросклероза [7, 10, 11]. Увеличение концентрации холестерина (ХС) в клетках приводит к изменению состава, физических свойств и функций клеточных мембран: рецепторно-опосредованного эндоцитоза, реактивности мемб-раносвязанных ферментов, проницаемости мембран для ионов и метаболитов. Сохранение определенной концентрации ХС плазматических мембран обеспечивает необходимое постоянство физических свойств и физического состояния бислоя мембран нормально функционирующей клетки, что лежит в основе холестеринового гомеостаза и поддерживается равновесием поступления и выведения ХС из организма.
Эта цель определяет основные задачи терапии: нормализацию массы тела с помощью диеты и физических нагрузок; отмену гепа-тотоксичных препаратов; нормализацию показателей углеводного, липидного и пуринового обмена; увеличение содержания в гепато-цитах аминокислот, необходимых для синтеза апопротеинов, и ко-ферментов для синтеза ЛПОНП; уменьшение эндотоксемии; нормализацию активности процессов ПОЛ; выведение токсических метаболитов; ингибирование воспаления в ткани печени и т.д.
Таблица 1. Динамика показателей биохимического анализа крови у больных первой группы (принимавших таурин (Дибикор))
Лецитин. Чем помогает и как принимать
Порошковый лецитин считается одной из самых полезных добавок для здоровья. Но мало кто знает, насколько широка его сфера применения! О том, чем полезен, какой выбрать и как принимать лецитин пойдет речь ниже.
История появления лецитина
Впервые его открыл ученый из Франции Т. Гобли, который в 1845 году выявил схожесть в составе тканей мозга и яичного желтка. По его теории, которая вскоре была доказана, именно лецитин является объединяющим компонентом. Он на 75% состоит из фосфолипидов, триглицеридов, это жироподобное вещество. Именно фосфолипиды являются составляющими клеточных мембран, они содержаться в большинстве живых организмов и тканей. Так, их очень много в тканях мозга, печени, плазме крови, сердца, желчи.
Современные источники лецитина
Из чего состоит лецитин
В нем гармонично сочетаются 4 формы фосфолипидов:
Таким образом, лецитин это не один ингредиент, как думают многие. А целый комплекс, смесь ценных фосфолипидов, которые по-своему влияют на организм человека.
Общая полезность
Как уже было сказано, фосфолипиды составляют структуру клеточных мембран, участвуют в большинстве процессов в организме. Кроме того, лецитин очень полезен для печени, поскольку содержит фосфатидилхолин, составляющее печеночных клеток. Когда печень болеет, мембраны клеток разрушаются, а лецитин и ее компоненты восстанавливают их.
Кроме того, это вещество обладает хорошими антиоксидантными свойствами и действует на клетки печени как детокс. Важно! Лецитин, в большем или меньшем количестве, входит в состав большинства аптечных гепатопротекторов (Эссенциале форте Н, Доппельгерц и другие). Это еще одно доказательство полезности его для печени.
Полезность лецитина для сосудов и крови
Вот кому особенно показаны биодобавки с лецитином
Есть ли противопоказания у лецитина
Поскольку это натуральная добавка, которую производят из сои или семян подсолнечника, она почти не имеет противопоказаний. Но лецитин стоит принимать с осторожностью или под контролем врача в таких случаях:
Беременным и кормящим можно принимать это вещество, но только после консультации со своим врачом.
Лецитин в порошке, таблетках или гранулах
Как принимать порошковый лецитин? Очень просто и удобно! Берем 1-2 ст. ложки порошка и смешиваем с любой свежеприготовленной пищей (обычно это каша, йогурт). Можно также просто запивать порошок водой или разводить в воде и сразу выпивать. Оставшуюся смесь нужно хранить в плотно закрытой банке, желательно на дверце холодильника, без перепадов температур.
Какие побочные действия возможны?
Как правило, при правильном, регулярном приеме их не наблюдается. Но в начале приема возможны некоторые кратковременные расстройства:
Обращайте внимание на эти симптомы! Они должны пройти через 1-2 дня после начала приема препарата. Если этого не случилось, прекратите прием и обратитесь к врачу. Еще один возможный симптом: кожный зуд, насморк могут быть признаком аллергии на лецитин или другие компоненты. Прием в этом случае нужно прекратить.
Заключение
10 ошибок, которые совершают люди при приеме витаминов, микроэлементов и БАДов
Как принимать витамин Д, Омегу-3 и железо, чтобы извлечь из них пользу, а не вред? Почему стоит внимательно изучать состав спортивных БАДов? Что еще кроме гиалуроновой кислоты и коллагена полезно для нашей кожи? Врач высшей категории, эндокринолог Либеранская Наталья Сергеевна делится полезными рекомендациями, которые помогут справиться с сезонным авитаминозом и сохранить здоровье.
Ошибка №1. Не контролировать уровень витамина Д
Витамин Д положительно влияет на инсулинорезистентность и обмен веществ, способность организма противостоять ОРВИ и окислительному стрессу, снижает риск развития онкологических заболеваний и отклонений в развитии плода во время беременности. Более того, «солнечный» витамин Д помогает не хандрить и снижает болевые ощущения во время родов.
В регионах с низким уровнем инсоляции (к ним относится Санкт-Петербург) дефицит витамина Д крайне распространен. Однако принимать его в профилактических целях не стоит, поскольку витамин Д – это все-таки стероидный гормон. Только после специального лабораторного анализа крови на Д-гормон можно узнать его уровень в организме, после чего корректировать дефицит.
Ошибка №2. Принимать кальций без нормализации витамина Д и магния
Кальций — важный минерал, который поддерживает хорошее состояние костей и зубов, отвечает за свертываемость крови и рост, поддерживает тонус мышц и нервной системы. Достаточное поступление кальция необходимо для профилактики и лечения остеопороза, а также артериальной гипертензии.
Но кальций не усваивается, если в организме есть дефицит витамина Д и магния. Принимать кальций в этом случае просто бессмысленно.
Ошибка №3. Не знать, какой витамин Д принимать
Холекальциферол — неактивная форма витамина Д, именно она нужна для коррекции его дефицита, чтобы все системы организма работали исправно, и вы чувствовали себя хорошо. Препарат холекальциферола безопасен — вероятность передозировки мала. Но есть другая, активная форма витамина Д — кальцитриол. Его можно принимать только под контролем врача и по медицинским показаниям.
Ошибка №4. Принимать витамин D — не всегда значит нормализовать его уровень
Витамин D плохо усваивается в следующих ситуациях:
Ошибка №5. Игнорировать Омега-3
Для чего принимают Омега-3 полиненасыщенную кислоту? Она сохраняет остроту зрения, красоту и защищает эндотелий сосудов от повреждений. головной мозг на 30% состоит именно из Омега-3 жирных кислот. Вещество не синтезируется в организме самостоятельно. К сожалению, даже приверженцы Средиземноморской диеты не всегда получают достаточное количество Омега-3. Жирная кислота содержится в жирной рыбе, льняном, облепиховом и горчичном маслах.
Взрослым ежедневно следует принимать 2 г Омега-3 — и даже больше.
Точная дозировка может быть подобрана после анализа, который называется Омега-3 индекс.
Преимущество Омега-3 в капсулах перед той же красной рыбой заключается в хорошей очистке жирных кислот от вредных примесей, которые мы можем получать вместе с рыбой, пойманной в водоеме.
Ошибка №6. Не различать Омега-3 и Омега-6
Омега-3 и Омега-6 относятся к полезным и важным для организма ненасыщенным жирным кислотам. Однако принимать Омега-6 дополнительно нет необходимости — этот компонент мы в достаточном количестве получаем из пищи из растительных масел, мяса птицы, овсянки и др. Избыток Омега-6 может сыграть на руку воспалительным процессам в организме.
Ошибка №7. Игнорировать железо (ферритин)
Дефицит железа приводит к анемии, быстрой утомляемости, мышечной слабости, сухости кожи, выпадению волос. Женщины находятся в группе риска по потере железа из-за менструации, не получают нужное количество этого микроэлемента и вегетарианцы.
Ошибка №8. Принимать железо вслепую
В плане усвоения железо — особенно капризный микроэлемент. Принимать его следует особенно осторожно. Дело даже не в том, что препарат в каплях окрашивает зубную эмаль. Избыток железа откладывается во внутренних органах (печень, поджелудочная, щитовидная железа), приводя к серьезным нарушениям: гемохроматозу, циррозу, гепатиту, меланодермии (пыльно-бронзовый цвет кожи).
Железо плохо усваивается с молочными продуктами и кофе.
Напротив, витамин С, В12, фолиевая кислота способствуют благоприятному усвоению железа.
Если железо усваивается плохо, врач назначает специальные комплексы.
Ошибка №9. Спортивные БАДы — доверять и не проверять
Некоторые спортсмены для ускорения роста мышц и «сушки» принимают протеины. Одним из самых популярных сегодня является казеин, который изготавливается из обыкновенного коровьего молока. Протеин казеин — дешевый в производстве, однако подходит он далеко не всем. Чем вреден казеин? Попадая в организм, он превращается в казоморфин, который вызывает привыкание, может провоцировать воспаления слизистой кишечника, аутоиммунные заболевания, отечность и заторможенность.
Протеин казеин не следует принимать тем, у кого есть проблемы с ЖКТ, а также индивидуальная непереносимость лактозы и казеина.
Ошибка №10. Для кожи полезны не только коллаген и гиалуроновая кислота
После 35-40 лет кожа стареет. У многих женщин наблюдается недостаток пептидов коллагена и гиалуроновой кислоты: в этом случае на помощь приходит инъекционная косметология и капсулы — в качестве вспомогательного метода борьбы с признаками возрастных изменений.
Однако для кожи полезны и другие компоненты:
Консультация эндокринолога — вектор вашего внутреннего баланса!
Либеранская Наталья Сергеевна — эндокринолог, врач высшей категории с опытом работы более 10 лет. Наталья Сергеевна принимает пациентов с самыми разными проблемами и вопросами в рамках своей специализации — избыточный вес, сахарный диабет, проблемы с щитовидной железой, повышенная утомляемость и сонливость, беременность, менопауза, нарушение обмена веществ и работы эндокринных желез.
Наталья Сергеевна — автор популярного блога @doctor_liberanskaya, в котором регулярно дает подписчикам советы по поддержанию здоровья и терапии. Все рекомендации основаны на принципах научно-доказательной медицины и собственного профессионального опыта.
С 2017 года доктор Либеранская Наталья Сергеевна принимает пациентов в клинике Пирогова — вы тоже можете пройти консультацию эндокринолога высшей категории.
Пройти обследование быстро, без очередей и в удобное для вас время можно и в нашей клинике. Благодаря новейшему диагностическому оборудованию и команде квалифицированных специалистов лаборатории клиники Пирогова, вы можете быть уверены в объективных и достоверных результатах.